Mieux connaitre le pouvoir pathogène des champignons
Travail de Pascale Naim
a. Cycle de vie de la Tavelure et facteurs climatiques.
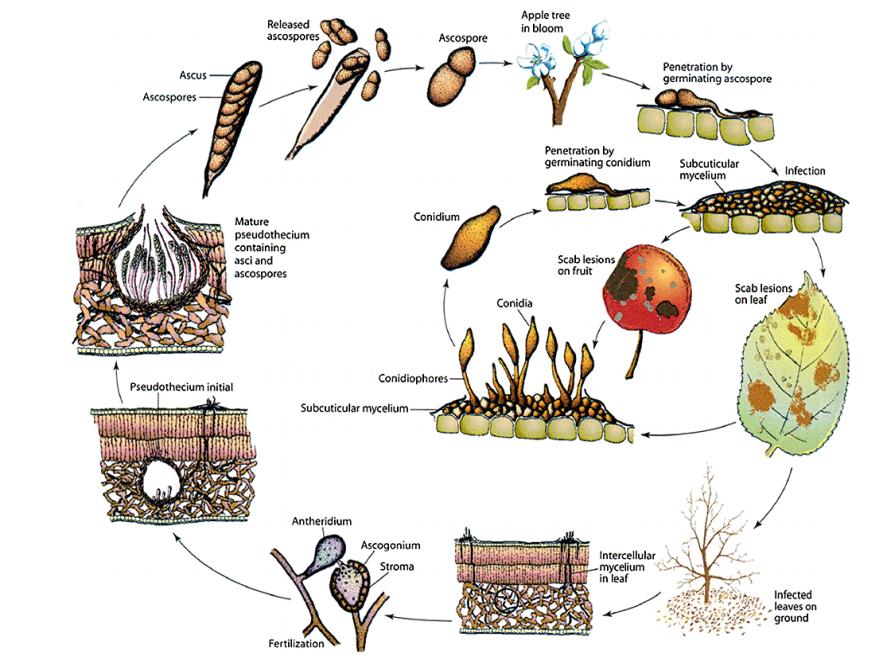
Cycle de vie de Venturia inaequalis (tiré de Bowen et al., 2011)
Le développement du mycélium de Venturia inaequalis nécessite la présence d'ascospores dans de l'eau pendant une durée assez longue, autrement dit une durée d'humectation suffisante, pour pénétrer la cuticule et causer l'infection primaire de l'organe (feuille ou fruit). L'infection secondaire repose sur le même principe et les conidies nécessitent une humectation plus longue que les ascospores pour qu'il y ait succès de l'infection.
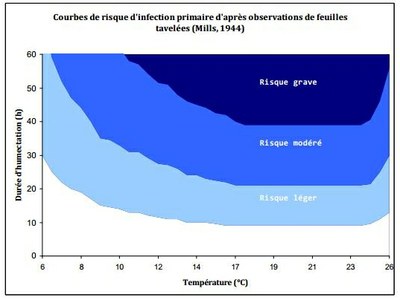
Les travaux de Mills dès la fin des années 1930 se sont ainsi portés sur la mise en place de tables déterminant à une température donnée la durée d'humectation nécessaire à l'infection.
- Les courbes de risque d'infection en fonction de la température et de la durée d'humectation selon les critères de Mills déterminent la sévérité du risque.
Venturi inaequalis est un champignon hémibiotrophe ( infectant les tissus vivants d'un organisme et poursuivant son développement sur les tissus morts) dont le mycélium se développe exclusivement entre la cuticule et les cellules de l&rsqursquo;épiderme de la feuille ou du fruit.
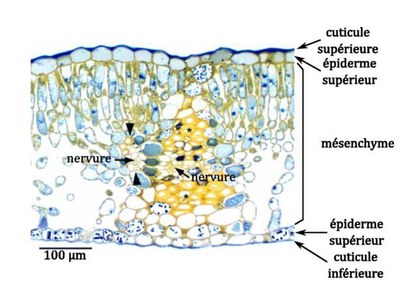
Coupe transversale d'une feuille de pommier – d'après (Reidel et al., 2009)
b. Pouvoir pathogène de Venturia inaequalis.
40 % des traitements servent à contrôler la seule tavelure du pommier : Venturia inaequalis, champignon ascomycète
Il passe l’hiver sous forme de périthèces, des organes de reproduction sexuée, dans la litière des feuilles mortes tombées au sol. Au printemps, lorsque la température et l’humidité sont favorables, les ascospores produites par les périthèces, sont libérées, puis projetées par les éclaboussures de pluie ou portées par le vent sur les organes verts des pommiers. Ces ascospores vont alors développer un tube germinatif qui va traverser la cuticule des tissus soit directement soit à l’aide d’un appressorium
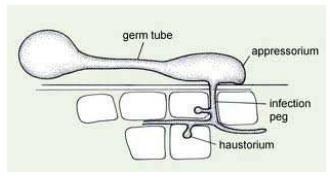
Pénétration du champignon dans les tissus végétaux par un appressorium ( Bowen et al., 2011).
Venturia inaequalis est un champignon de spectre géographique large, présent dans presque tous les vergers commerciaux. Ce champignon tue rarement son hôte, mais un niveau d’infection très bas suffit à rendre les pommes non commercialisables, il est donc important de connaitre le pouvoir pathogène du champignon.
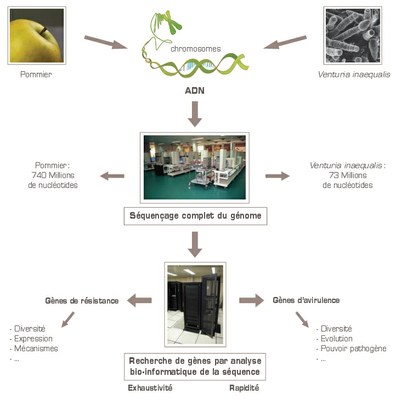
La tavelure et les pommiers ont évolués conjointement depuis la domestication du pommier en Asie il y a environ 5000 ans. Identifier les gènes impliqués dans l'interaction entre l'hôte et le pathogène permettrait de mieux comprendre le pouvoir pathogène de la Tavelure. Les chercheurs de l’INRA essaient actuellement de comparer les génomes actuels du champignon d’une part, du pommier d’autre part, avec ceux de leurs ancêtres respectifs, que l’on trouve encore au Kazakhstan et en Chine occidentale. Ils disposent en effet des séquences complètes des génomes des deux partenaires.
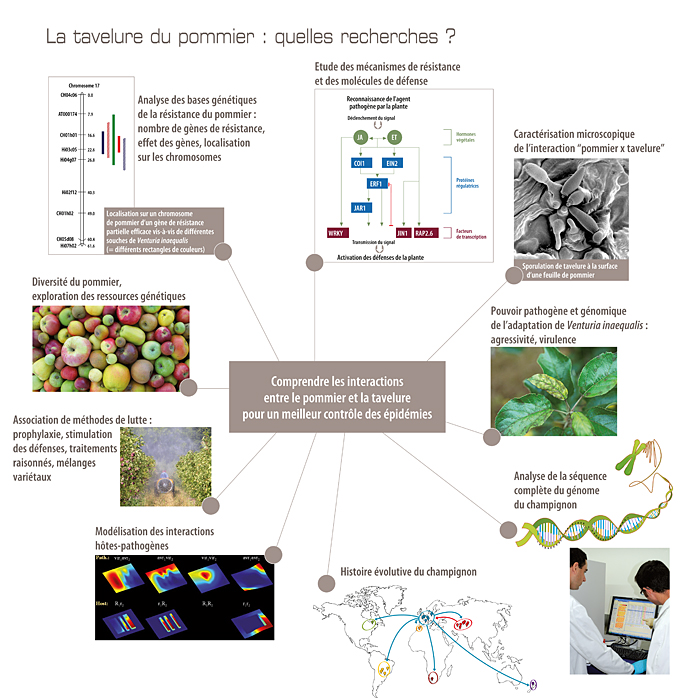
- La résistance hôte est exprimée par certains génotypes d’une même espèce végétale, par ailleurs sensible, soit envers tous les génotypes connus d’un agent pathogène donné (résistance non spécifique) soit envers certains génotypes de cet agent pathogène (résistance spécifique). Cette résistance est dite induite car elle est déclenchée par l’attaque de l’agent pathogène, ce qui implique une reconnaissance de ce dernier (ou des perturbations métaboliques qu’il provoque) par la plante.
- La résistance des plantes est souvent contrôlée par des gènes conférant de hauts niveaux de résistance (résistance totale, le plus souvent) mais seulement envers certains génotypes pathogènes : on parle de résistance qualitative race-spécifique. Ce type de résistance est à hérédité mendélienne et sous le contrôle d’un seul gène (résistance monogénique) : la présence de l’allèle favorable confère la résistance, et réciproquement, l’allèle défavorable entraîne la sensibilité.
Ces résistances monogéniques qualitatives sont faciles à sélectionner dans les descendances de croisements, d’où leur large utilisation dans la création des nouvelles variétés résistantes. De plus, les gènes contrôlant ces résistances, aussi appelés gènes majeurs (ou R-genes en anglais), peuvent être facilement positionnés sur une carte génétique au voisinage de marqueurs moléculaires. Une résistance efficace n’est déclenchée que si l’agent pathogène possède l’allèle d’avirulence ( Avr) qui est reconnu par un allèle de résistance (R) de la plante hôte. Si l’un ou les deux partenaires possèdent les allèles non fonctionnels ou récessifs, la maladie se développe.
|
|
|
Plante (pommier)
|
|
|
|
&nbnbsp;
|
Résistance (RR ou Rr) |
Sensible (rr) |
|
Pathogène
(Tavelure)
|
Avirulent (Avr) |
Résistance
|
Maladie
|
|
Virulent (avr) |
Maladie
|
Maladie
|
|
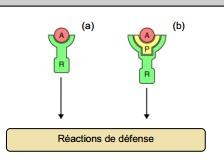
Interprétation biochimique du modèle.(d’après Bonas et Lahaye 2002)
· (a) interaction directe entre une protéine codée par le gène d’avirulence A de l’agent pathogène et une protéine codée par le gène de résistance R de la plante hôte.
· (b) Une protéine A se fixe sur une cible moléculaire P de la plante hôte, et ce complexe se fixe sur la protéine R.