Le gène RB : exploitation pédagogique
Le gène RB : exploitation pédagogique
![]() Document « Les caractéristiques du rétinoblastome »
Document « Les caractéristiques du rétinoblastome »
On peut demander aux élèves de :
- dégager les caractéristiques communes à tous les rétinoblastomes ;
- discuter du caractère héréditaire ou non de ce type de cancer chez les familles A et B ;
- proposer une explication aux caractéristiques du cancer dans la famille C.
Le document permet d’abord de dégager les caractéristiques communes à tous les rétinoblastomes : c’est un cancer qui apparait précocement, avant l’âge de 5 ans, et qui se traduit par au moins une tumeur à l’intérieur d’un œil. Cette tumeur a pour origine une cellule de la rétine qui, au cours du développement, au lieu de se différencier (en cellule photo réceptrice par exemple) a conservé un caractère embryonnaire et s’est multipliée de façon incontrôlée.
Les arbres généalogiques permettent de reconnaître deux formes de rétinoblastome. Dans l'une de ces formes, la forme A, on constate la présence de personnes atteintes dans plusieurs générations de la famille (cela suppose que les personnes atteintes aient été bien soignées pour atteindre l’âge adulte). Vu que le rétinoblastome est un cancer rare dont la fréquence est estimée à 1/20.000, cela signifie que le rétinoblastome dans une telle famille est héréditaire.
Dans la forme B, le sujet atteint apparaît au sein d’une famille où on ne connaît pas de cas de rétinoblastome. C’est d’ailleurs la forme la plus fréquente (60% des cas environ). La personne atteinte n’a pas d’individus affectés dans sa descendance. On parle de rétinoblastome sporadique, non héréditaire.
L’arbre généalogique C est une variante de rétinoblastome héréditaire où il n’y a pas de personnes atteintes dans l’ascendance du premier sujet atteint mais où on en trouve dans la descendance de ce dernier. Il est intéressant de demander aux élèves une explication dans le cadre d’une hypothèse où un seul gène est en cause. Ils doivent imaginer une mutation de novo dans la lignée germinale d’un des parents du premier sujet atteint.
On peut alors faire le point sur les différences phénotypiques entre les deux formes de rétinoblastome. Le rétinoblastome héréditaire apparaît en moyenne plus précocement que le rétinoblastome sporadique.
Enfin le rétinoblastome héréditaire affecte souvent les deux yeux et il peut y avoir plusieurs tumeurs dans le même œil. Comme la tumeur a pour origine une seule cellule, cela signifie que plusieurs cellules sont devenues cancéreuses dans le cas du cancer héréditaire ce qui n’est pas le cas avec le rétinoblastome sporadique.
![]() Document « Origine du rétinoblastome »
Document « Origine du rétinoblastome »
On peut demander aux élèves d'analyser les données génétiques relatives aux membres des 3 familles afin de :
- discuter de la validité ou non de l'hypothèse de Knudson ;
- confirmer ou non les conclusions précédentes sur le caractère héréditaire ou non du cancer du rétinoblastame dans les familles A et B ;
- valider ou non l'interprétation fournie prédédemment pour expliquer les caractéristiques de la transmission du cancer dans la famille C et de là dégager la notion de mutation germinale ;
- montrer qu'une mutation germinale est intervenue dans l'histoire de la famille A ;
- montrer que des mutations somatiques interviennent dans tous les rétinoblastomes ;
- proposer un schéma synthétique sur les mécanismes héréditaires et non héréditaires dans le cas du cancer du rétinoblastome.
C’est à partir d’un traitement statistique des données sur les divers aspects du rétinoblastome (trop complexe pour être abordé avec des élèves de lycée), que Knudson a proposé une hypothèse sur les mécanismes génétiques à l’origine du rétinoblastome.
L’hypothèse de knudson repose sur l’idée qu’un seul gène est en jeu et que c’est le même dans les deux cas de rétinoblastome héréditaire et non héréditaire. Surtout, elle suppose que les deux allèles du gène sont mutés dans le cas d’une cellule tumorale. Le génotype d’une cellule atteinte du rétinoblastome suppose donc l’existence de deux mutations, une pour chaque allèle (d’où l’expression « Two hit hypothesis »).
Durant les années 70 et 80 les recherches se sont poursuivies sur le rétinoblastome jusqu’à aboutir à l’isolement du gène en 1986 et son séquençage en 1987. Après, on a recherché les diverses mutations en cause. Ce sont quelques-unes de ces mutations qui ont été utilisées pour établir les génotypes de quelques individus des arbres généalogiques. Pour les individus atteints, on a fourni dans les fichiers des séquences des familles le génotype des cellules cancéreuses et celui des cellules saines.
La comparaison des allèles Rb de chacun des individus des 3 familles avec l'allèle de référence montre que toutes les cellules cancéreuses ont deux allèles mutés. ce qui confirme l'hypothèse de Knudson.
Dans le cas de la famille A, on constate que chez une personne atteinte de rétinoblastome, les cellules cancéreuses ont deux allèles mutés et les cellules saines ont un allèle muté et un allèle non muté. En outre un des allèles mutés des cellules cancéreuses est le même que celui trouvé dans les cellules saines. Cela signifie qu’un des allèles mutés a été fourni par un gamète d’un des parents, celui atteint de rétinoblastome, et que le deuxième allèle muté dans les cellules cancéreuses provient d’une mutation somatique apparue dans une cellule rétinienne. En conclusion, cela confirme le caractère héréditaire du rétinoblastome dans cette famille.
Pour le cancer de la famille B, les individus atteints ont deux allèles mutés dans les cellules cancéreuses, souvent deux allèles différents et deux allèles non mutés dans les autres cellules du corps. Cela confirme l'idée d'un cancer non héréditaire.
Remarque :
Dans les familles avec rétinoblastome héréditaire, il se peut qu'un individu possède dans toutes ses cellules un allèle muté hérité de l'un des parents et un allèle normal (10 % des cas, non illustré dans l'arbre de la famille A) sans être atteint de rétinoblastome. C'est pourquoi on devrait parler de la transmission d'une prédisposition au rétinoblastome et non de l'hérédité du rétinoblastome. Dans 90% des cas, un tel génotype entraîne l'apparition d'un rétinoblastome. Autrement dit, la probabilité pour qu’un individu ayant dans son génotype un allèle muté et un allèle non muté ne soit pas atteint est très faible (mais non nulle). Si les cellules rétiniennes ont hérité d’un allèle muté, la probabilité pour qu’une mutation intervienne sur l’autre allèle pour une ou quelques-unes des cellules rétiniennes (au nombre de 120 millions environ) est donc très forte mais elle n'est pas de 100%. Les mécanismes qui font que la possession d'un allèle muté prédispose à une mutation de l'allèle normal sont variés et complexes (mutations ponctuelles comme illustré, délétion, conversion de l'allèle normal en allèle muté, etc.). C’est ce qui explique la possibilité de plusieurs tumeurs dans le cas d’un rétinoblastome héréditaire. Et dans le cas d'un rétinoblastome héréditaire, on a remarqué aussi que la fréquence d’autres cancers, notamment d’ostéosarcomes, est par la suite augmentée.
Dans le cas de la famille C, les parents du premier individu atteint d’un rétinoblastome (III1) possèdent dans toutes leurs cellules deux allèles « normaux » du gène RB ce qui est conforme avec le fait qu’ils n’ont pas été atteints par ce type de cancer durant leur enfance. Cependant leur fils possède dans toutes ses cellules non cancéreuses un allèle muté. Cela signifie que cet allèle muté était présent dès le stade œuf. Il l’a hérité d’un des gamètes qui lui a donné naissance. Il y a donc eu une mutation germinale affectant le gène RB chez un des parents (mutation de novo). A partir de là, la prédisposition au rétinoblastome devient héréditaire dans la famille comme l’illustrent III1 et III3.
L'analyse des séquences des membres de la famille A ne met pas en évidence de mutation germinale mais seulement la transmission d'un allèle muté de génération en génération. Cependant, dans l'ascendance de cette famille, il a dû y avoir à un moment donné une mutation germinale (mutation de novo) qui explique qu'un allèle muté soit présent dans toutes les cellules de la femme I1.
En conclusion, les mutations somatiques sont toujours en jeu dans les rétinoblastomes : 2 mutations somatiques dans le cas des rétinoblastomes sporadiques non héréditaires, 1 mutation somatique en plus de l'allèle muté hérité dans le cas des rétinoblastomes héréditaires.
Les figures ci-dessous illustrent les représentations possibles.
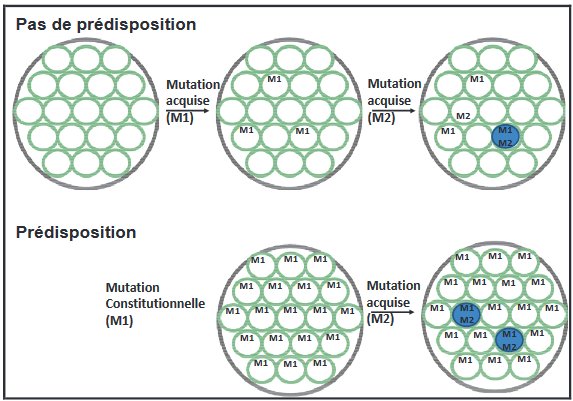
Figure 3 d'après : Etude des relations génotype phénotype dans le rétinoblastome Laurent Castera. Ici sont schématisées des rétines (grands cercles) et des cellules rétiniennes (petits cercles). Les tissus prédisposés portent la première mutation (M1) inactivant le premier allèle dans toutes les cellules. L’apparition d’une deuxième mutation (M2) inactivant le deuxième allèle d’un gène Rb initie le développement d’un rétinoblastome (cercle bleu).
La figure ci-dessous résume les mécanismes causes du rétinoblastome héréditaire et non héréditaire.
.
D'après The Cell: A Molecular Approach. Geoffrey M Cooper. Boston University. Sunderland (MA) : Sinauer Associates; 2000.
