Interview d'Isabelle Lacroix, Laboratoire Pasteur-Cerba
Isabelle Lacroix, médecin biologiste responsable des analyses sériques du dépistage de la trisomie 21 au Laboratoire Pasteur-Cerba, Saint-Ouen Liesse, est interviewée par Françoise Jauzein, le 2 septembre 2004.
Voir les photos de la visite du laboratoire.
Dix mille échantillons environ arrivent tous les jours au laboratoire (en fait toutes les nuits), de France, Outre-mer, Afrique …) . Cela correspond en général aux analyses que les biologistes de ville ou les hospitaliers ne peuvent pas faire, dans divers domaines : infectieux, biologie moléculaire, hormoneo spécialisée, hémato….. Techniques pratiquées : Elisa, radio-isotopes, biologie moléculaire (mais pas les analyses de produits dopants qui sont pratiquées par des labos particuliers (labos indépendants, agréments spécifiques), ainsi que dans les cas d’accident, pour la confirmation de dépistages de neuroleptiques qui demande de la spectrométrie atomique.
Le laboratoire emploie 450 personnes, et comprend 4 départements
Biologie humaine spécialisée
Anatomo pathologie
Génétique (oncogénétique, cytogénétique, biologie moléculaire, réalisées sur du liquide amniotique)
Santé animale (ESB sur des troncs cérébraux bovins, tests réalisés la nuit, le résultat envoyé à 6h du matin permet de "libérer" les carcasses bovines pour les boucheries)
ainsi que divers services (documentaires, commercial, achats, généraux, ressources humaines.
Les collectes des échantillons à traiter sont sous-traitées avec la société Ariatime, 80 agents récupèrent en voiture (territoire français dividé en 6 zones géographiques) les échantillons dans les laboratoires de province. Ceux-ci (ainsi que ceux arivant par avion des DOM-TOM) sont stockés dans les terminaux de frets aériens ou routiers aux températures adéquates (+4°C, -20°C et Ture ambiante). Les échantillons arrivent au labo à 6heures du matin et les analyses sont effectuées dans la journée. Les résultats sont imprimés et les dossiers mis sous plis le soir pour repartir en province avec les malles de collectes réfrigérées. Des lignes sécurisées existent pour les transferts rapides de résultats aux biologistes (2/3 pharmaciens et 1/3 médecins).
Les pionniers du dépisage de la trisomie 21 sont les anglais. Ils avaient une grosse prévalence des pathologies de la non fermeture du tube neural (NFTN), (anencéphalies et spinna bifida), notamment par manque de légumes verts non cuits (source d'acide folique) dans l'alimentation. Dans les années 80 , ils remarquèrent que l'AFP était très élevée chez ces gens et ils mirent en place un dépistage par dosage sanguin de l'AFP lors du deuxième trimestre de la grossesse (l'échographie du premier trimestre n'avait pas, à cette époque, une resolution suffisante pour déceler ces anomalies morphologiques). Parmi les femmes enceintes d'enfants porteurs d'un spina, 90% présentent un taux d'AFP supérieur à 2,5 MOM. Ils mirent alors par hasard, en évidence, une corrélation entre des valeurs faibles du taux d'AFP sérique maternelle et la présence d'une grossesse trisomique. Les sérothèques furent alors reprises et les analyses des hormones hCG et E3 (unconjugated oestradiol),les seules possibles à l'époque, furent refaites systématiquement.
C'est Wald (un anglais), qui, le premier, eut l'idée de mettre au point un logiciel associant différents facteurs (âge maternel et diifférents marqueurs; en réalité 3: le fameux triple-test anglais) pour évaluer le risque de trisomie 21 en cours de grossesse.
Bienqu'ils aient été les pionniers en matière de dépistage de T21, les anglais n'ont toujours pas de cadre legislatif. La France est le seul pays qui s'en soit doté, et encore celui-ci ne concerne -t-il que les marqueurs sériques du deuxième trimestre (entre la 15ème t la 18ème SA, avec remboursement du test sérique, contrôle de qualité et "cut-off" (seuil de risque) à 1/250.
Avant la circulaire de 1997, les dosages hCG et E3 étaient cotés B250 et remboursés, mais l'amniocentèse ne l'était pas. De façon à diminuer l'inégalité d'accès au diagnostic, une association loi 1901 demandaient aux femmes de payer 450FF: 300F remboursés (pour les marqueurs sériques) et 150F de plus pour payer les amniocentèses aux femmes les plus démunies. En Angleterre, où il n'y a pas de cadre légal, le remboursement de deux marqueurs est tout de même prévu , mais il faut payer de sa poche si on en veut 4.
En France, avant la mise en place du dépistage actuel, on ne pratiquait que le dosage de l'hCG. C'est le laboratoire Cerba qui a démarré le premier la pratique du triple test, sans directives ministérielles. Dans le cadre d'une étude coût/efficacité, les résultats de Cerba ont été testés avec 1,2 ou 3 marqueurs. Suite à cette étude l'état a décidé la mise en place du dépistage tel qu'aujourd'hui, avec deux marqueurs. Au début les laboratoires de l'assistance publique, faute de moyens (F Müller, 1997) n'utilisaient qu'un seul marqueur.
Au cours d'un congrès, en mai 2003, les chiffres suivants furent donnés: en Angleterre moins de 40% des femmes enceintes faisaient le dépistage alors qu'en France, 80% des femmes (tous âges confondus) le faisaient.
Pour le dépistage des malformations foetales, chromosomiques ou morphologiques, la France se place actuellement dans les tous premiers pays au monde, les pouvoirs publics ont en effet relayé la volonté médicale de dépistage, sous la forme de prises en charge et de recommandations multiples: remboursemnt de trois echographies au cours de la grossese, remboursement et obligation de proposition de dépistage de la T21 par les marqueurs sériques chez toutes les femmes enceintes (avec protocole de consentement), remboursement et obligation de proposition d'amniocentèse aux femmes enceintes de plus de 38 ans, dotations budgétaires pour les services de génétique clinique, interruption médicale de grossesse autorisée sans exigence de certitude diagnostique, quel que soit le terme de la grossesse (après réunion d'un conseil génétique).
Les diverses indications de caryotype sont les suivantes:
Antécédent de trisomie 21
Anomalie décelée à l'échographie du 1er, 2ème ou 3ème trimestre
Age de la mère supérieur à 38 ans à la date de l'amniocentèse
Dépistage de maladies liées au chromosome X
Valeur de risque evalué par le test sérique supérieur à 1/250, au moment du prélèvement sanguin (et non à terme comme dans d'autres pays)
Remarque: certains pays travaillent avec un cut-off de 1/250 à terme, ce qui représente une plus faible population de femmes à qui l'on proposera l'amniocentèse (sur les 7% de femmes qui se la voient proposer, cela représente 20% de femmes en moins).
La femme de 38 ans a donc le choix entre une amniocentèse directement, ou une étude de ses marqueurs sériques, qui ouvrira sur l'alternative d'amniocentèse ou pas.En France l'amniocentèse est remboursée pour les femmes de plus de 38 ans (à la date de prélèvement). Dans d'autres pays, cet examen est remboursé à partir de 35 ans. Le fait de placer le seuil de 1/250 au moment des MSM compense le non remboursement entre 35 et 38 ans, et s'avère plus efficace pour le dépistage.
L'attitude des medécins vis à vis de femmes enceintes, de plusde 38 ans, est variable:
soit ils proposent l'amniocentèse à toutes ces femmes
soit ils proposent le test sérique en premier
soit ils se fondent sur une échographie précoce à 12 SA
Parmi la population de femmes d'âge supérieur à 38 ans, 1/3 environ aura une évaluation du risque par les MSM supérieure à 1/250 et toutes les femmes à risque élevé feront une amniocentèse.Cela amènera à un taux de détection de la trisomie 21 de 95%. Les 5% de faux négatifs correspondent à des femmes classées à tord dans le groupe à risque faible (elles ont fait pratiquer une amniocentèse qui a montré une trisomie alors qu'elles avaient été classées dans le groupe à risque faible). Par contre on ne dispose pas de chiffres sur le nombre de femmes de plus de 38 ans qui font une amniocentèse, qu'elle aient un risque inférieur ou supérieur à 1/250.
En ce qui concerne le test sérique de l'hCG, plusieurs paramètres peuvent introduire un biais. Quand le foetus est une fille, l'hCG est satistiquement plus élevée et la grossesse est plus facilement placée dans le groupe à risque. De même une hypertension artérielle fait augmenter l'hCG. Enfin des modifications des marqueurs sériques signent en général une souffrance foetale. Une femme qui pésente un risque accru avec un caryotype normal, a de grandes "chances" d'avoir une pathologie foetale (petit poids à la naissance, HTA chez la mère, diabète gestationnel, hématome rétro-placentaire...sont associés à des modifications des marqueurs sériques) . En effet, les modifications des MSM observées dans les grossesses trisomiques reflètent une anomalie de développement du placenta , voir référence "Anomalie du développement placentaire lors de grossesses associées à une trisomie 21" de JL Frendo, en ligne à l'adresse suivante: http://www.performances-medicales.com/gyneco/Encours/77/article07.htm ).
Une formation des médecins est par ailleurs nécessaire pour une bonne compréhension des résultats, et le fait qu'ils interprètent notamment les valeurs des MSM en termes de MOM.
Les données concernant les pertes foetales varient d'une référence à une autre , de 0,5 à 2%, et l'habileté du praticien est souvent mise en cause. En fait, il est très diffcile d'estimer la part de responsabilité de l'acte invasif lié à l'amniocentèse pour la bonne raison que les foetus sur lesquels il est pratiqué, classés "grossesse à risque", sont souvent en souffrance, le geste ne faisant que se surajouter à une pathologie existante.
Par ailleurs les pertes foetales naturelles d'enfants atteints d'anomalies chromosomiques sont importantes.
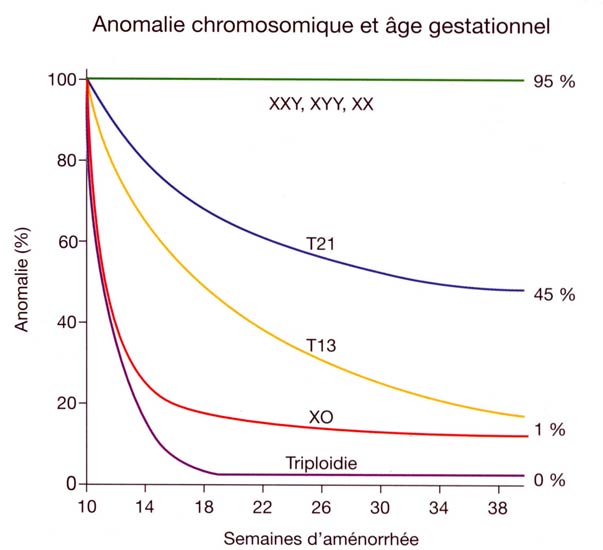 |
| Pertes foetales au cours de la grossesse pour divers types d'anomalies chromosomiques Ce graphique présente le risque relatif d'anomalies chromosomiques en fonction de l'âge gestationnel (par rapport au risque à 10 semines) La baisse du risque de présence d'une anomalie chromosomique s’explique par la perte spontanée de ces embryons au cours de la grossesse. Source: The 11-14 week scan, chapter 1.2: Calculation of risk for chromosomal defects, K.H. Nicolaides, N.J. Sebire, R.J.M. Snidjers http://www.fetalmedicine.com/11-14scanbook/Chapter1/chap01-2.htm |
Le caryotype montre en général une trisomie 21 libre mais quand il s'agit d'une translocation, elle est de type robertsonien: le chromosome 21 est fixé à l'un des chromosomes acrocentriques (13,14,15, 21 et 22), le plus souvent il s'agit de la 13/21.
Il existe principalement deux mécanismes d'apparition des rares cas de trisomie mosaïque. Soit celle-ci correspond à une "triplocation" du 21 au cours de mitose (mécanisme le plus classique), soit une trisomie exitait initialement dans l'oeuf et des mécanismes de correction ont réussi à la faire disparaître dans une cellule (et toutes sa descendance est alorsà 46K). Dans ce second cas, il y a, lors d'une deuxième grossesse, conservation du risque méiotique.
Dire que le phénotype ne dépend pas du pourcentage de cellules à 47K dans une personne portant une trisomie mosaïque doit être nuancé. Des tests d'expression génique pratiqués sur le peau, le placenta...ne montrent aucune relation , par contre il se pourrait qu'il y en ait pour des tissus comme le cerveau.....Par principe de précaution, lorsqu'on trouve une trisomie mosaïque on garde pour cette personne le même risque de maladie que s'il s'agissait d'une trisomie "classique". Il semble cependant qu'en ce qui concerne le risque de leucémie, important chez les personnes atteintes du syndrome de Down, un petit pourcentage de cellules normales dans le sang (10%) suffisent pour empêcher sn apparition.
Il n'y a pas d'encadrement juridique du dépistage échographique de la trisomie 21, par contre, il y a, depuis 1998, une obligation légale du renouvellement du parc échographique tous les 5 ans. Et depuis l'arrêt Perruche en 2000, il y a eu une réaugmentation des cotisations d'assurance des praticiens.
On assiste actuellement à une spécialisation de certains radiologues pour les échographies (le diplôme d'échographie est très récent et tout radiologue peut pratiquer des échographies).
La première échograpie, à 12 SA, faite avec des appareils de bonne qualité, doit permettre de réaliser une "mini-morpho", sur un foetus qui mesure entre 60 et 80mm (du même ordre de taille qu'un "Playmobil"), un certain nombre de caractères morphologiques (dont la CN, qui fait l'objet de recommandations), sont à observer.
Certains tests sont actuellement pratiqués sur les cellules foetales présentes dans le sang de la mère. Par exemple on peut réaliser une PCR pour chercher dans les cellules foetales une séquence d'ADN absente chez la mère; c'est ainsi que l'on peut chercher la séquence du gène SRY afin de savoir au plus tôt s'il s'agit d'un garçon dans les cas de certaines maladies génétiques. De même la recherche du rhésus sanguin de l'enfant (dans les cas de mère RH-) peut se faire sur les cellules foetales en circulation dans le sang maternel (mais n'est réalisé actuellement qu'à l'hopital américain de Paris) ou à partir de liquide amniotique. Ceci permet de limiter l'utlisation des gamma-globulines aux mères RH- portant un enfant Rh+, en relation avec le début de pénurie de ces produits sanguins . En bref, on peut faire les tests de biologie moléculaire concernant des gènes qui ne sont pas chez la mère. En cas de déficit en 21beta hydroxylase (enzyme surrénalienne dont l'inactivité provoque l'accumulation des androgènes et la masculinisation du foetus), on peut traiter le foetus à la dexaméthazone, dès la 13 ème semaine d'aménorrhée, puisque le SRY peut être décelé à partir du sang maternel à 10SA.
Pour diagnostiquer une trisomie, il faudrait pouvoir réaliser une étude quantitative, or le nombre de cellules foetales est faible dans le sang de la mère, et les techniques actelles ne permettent pas ce type d'analyse.
