Le carbone 14
Par ftrouillet
—
Dernière modification
19/09/2017 09:50
Le ![]() est un isotope radioactif du carbone qui se trouve en infime quantité dans le CO2 atmosphérique, les océans et la biosphère.
est un isotope radioactif du carbone qui se trouve en infime quantité dans le CO2 atmosphérique, les océans et la biosphère.
Découverte du carbone 14
- L'existence de cet isotope du carbone fut découverte par hasard en 1934 par l'américain Franz Kurie (Université de Yale) lors de l'exposition des noyaux d'azote à un flux de neutrons rapides.
- En 1940, les américains Martin Kamen et Samuel Ruben (Université de Berkeley) confirment son existence en mesurant l'activité du
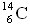 et sa période de demi-vie.
et sa période de demi-vie. - En 1940, l'américain Willard Frank Libby émet l'hypothèse d'une production continue de carbone 14 dans la nature en faisant le raisonnement suivant : puisque la période de demi-vie du
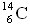 est de 5000 ans environ, cet isotope devrait avoir disparu depuis longtemps s'il n'était produit en continu.
est de 5000 ans environ, cet isotope devrait avoir disparu depuis longtemps s'il n'était produit en continu. - De 1940 à 1946, Libby établit les bases théoriques et pratiques de son utilisation pour effectuer des datations en archéologie. En 1947, il publie un article dans la revue Science révelant au public ses travaux tenus secrets jusque là, et proposant une méthode de datation.
- En 1949, la première datation d'un morceau de bois provenant d'une tombe égyptienne datée est expérimentée. C'est un succès et une véritable révolution pour l'archéologie.
- Willard Frank Libby obtiendra le prix Nobel de chimie en 1960 pour ses travaux.
Origine du carbone 14
- Le carbone
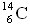 est produit dans la haute atmosphère (entre 7 000 et 12 000 m d'altitude) par une irradiation due aux rayons cosmiques. Les protons d'origine cosmique, non deviés par le champ magnétique terrestre et arrivant à pénètrer dans l'atmosphère donnent naissance à des neutrons. Ces neutrons, une fois ralentis, réagissent avec des noyaux d'azote pour former du carbone 14.
est produit dans la haute atmosphère (entre 7 000 et 12 000 m d'altitude) par une irradiation due aux rayons cosmiques. Les protons d'origine cosmique, non deviés par le champ magnétique terrestre et arrivant à pénètrer dans l'atmosphère donnent naissance à des neutrons. Ces neutrons, une fois ralentis, réagissent avec des noyaux d'azote pour former du carbone 14.
Devenir du carbone 14
- Le carbone
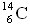 est rapidement oxydé par le dioxygène de l'air pour former du dioxyde de carbone 14CO2.
est rapidement oxydé par le dioxygène de l'air pour former du dioxyde de carbone 14CO2. - Le 14CO2 est absorbé par les végétaux chlorophylliens au cours de la photosynthèse. De fait, le carbone 14 va se répandre dans la biosphère tout au long de la chaîne alimentaire : on le retrouve donc dans tous les organismes vivants.
- Le 14CO2 circule dans l'atmoshère et se dissout dans les océans pour former des carbonates. On retrouve donc du carbone 14 dans les océans.
- Le rapport de populations de
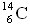 et de
et de 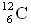 total est noté r0. Il vaut :
total est noté r0. Il vaut :
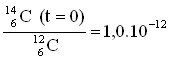
- Ce rapport est considéré comme uniforme dans l'atmosphère, la surface des océans et la biosphère en raison des échanges permanents entre les organismes vivants et leur milieu.
- Après la mort, le carbone 14 cesse d'être absorbé. De fait, sa proportion diminue car les noyaux de
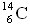 subissent des désintégrations radioactives
subissent des désintégrations radioactives  - :
- :
![]()
C'est ce qui permet de savoir depuis combien de temps l'organisme est mort.
Période de demi-vie
- La demi-vie de l'isotope
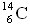 de l'élément carbone est en théorie de 5730 ans
de l'élément carbone est en théorie de 5730 ans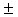
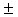 40 ans (valeur déterminée en 1962 par Godwin).
40 ans (valeur déterminée en 1962 par Godwin). - En 1950, une période de 5568
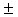 30 ans appelée "période conventionnelle" avait été déterminée par Libby. C'est cette période qui a été adoptée par la communauté scientifique et qui est utilisée par les laboratoires.
30 ans appelée "période conventionnelle" avait été déterminée par Libby. C'est cette période qui a été adoptée par la communauté scientifique et qui est utilisée par les laboratoires.
