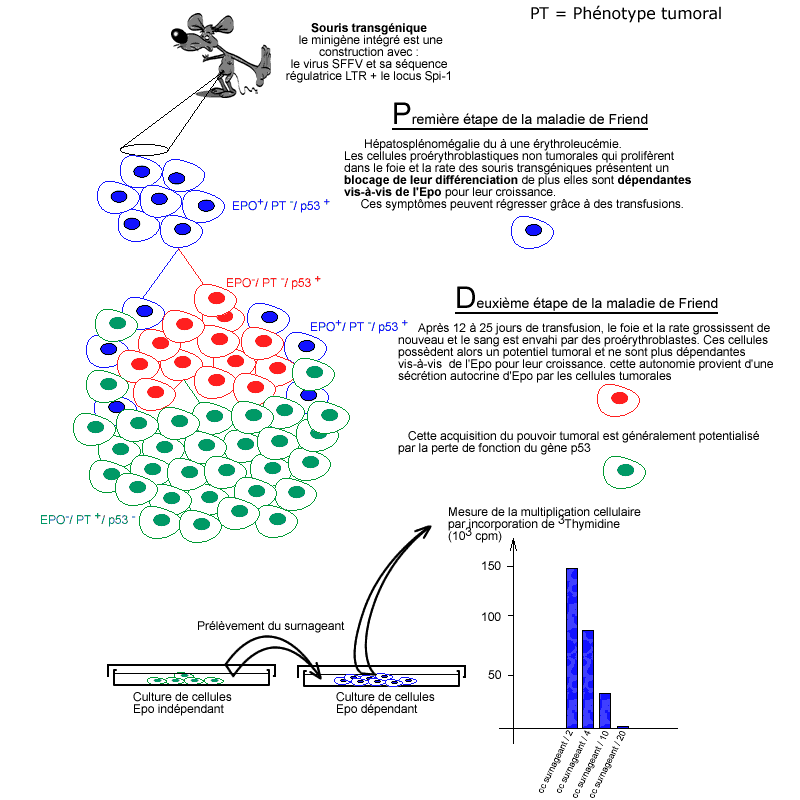
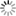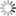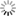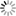Mécanismes de transformation tumorale
Transformation rétrovirale, le modèle des érythroleucémies de Friend
Le rétrovirus de Friend a été découvert par Charlotte Friend en 1957. Il est spécifique des souris et provoque différentes leucémies (érythroïdes, lymphoïdes …). Nous nous limiterons ici à l’étude des leucémies erythroïdes.
- L’érythropoïèse
Elle se déroule à partir de cellules souches se multipliant et se différenciant sous l'action de divers facteurs de croissance.
Les CFU-E subissent 4 cycles de divisions pour former des proérythroblastes. Toutes les étapes à partir de CFU-E sont EPO dépendantes.
Lors des érythroleucémies les proérythroblastes se multipliant vont migrer vers le sang périphérique car la moelle osseuse ne peut plus les contenir tous. Ainsi on retrouve des cellules nucléées dans le sang.
- Les rétrovirus de Friend
Il en existe deux catégories :
- Le Spleen Focus Forming Virus ou SFFV : il est défectif pour la réplication car il a besoin d’un autre virus pour se multiplier (en l’occurrence un FmuLV) et il est leucémogène aigu car il provoque une tumeur en 4 à 6 semaines.
Le rétrovirus
- La partie gag = environ 2 kb : protéines de la nucléocapside p15 – p12 – p30 – p10
- La partie pol = environ 3 kb :
RT (reverse transcriptase)
Rnase H (maturation du génome proviral)
Intégrase (intégration dans le génome de la cellule hôte)
p15E (dans l’enveloppe)
gp 70 (glycoprotéine de surface) permettant la reconnaissance de récepteurs
Cas du complexe rétroviral de Friend : FmuLV + SFFV
SFFV est certainement descendant de FmuLV en ayant subi des délétions
- à perte de séquence dans gag : il n’y a plus de protéine gag
- à perte dans pol : il n’y a plus de protéine RT
- à perte dans env : il n’y a plus de gp70 ni de p15E mais une protéine unique gp55
Il y a sans doute recombinaison avec le génome murin : une région spécifique du SFFV dans env (qui a un rôle dans la pathogénèse)
Physiopathologie de la maladie de Friend : SFFV + FmuLV
|
Souris Normale |
Souris Érythroleucémique |
|
|
Rate |
70 mg |
1500 mg |
|
Foie |
800 mg |
3500 mg |
|
Ganglions |
normaux |
Normaux |
|
Hématocrite |
45 – 50 |
75 – 80 |
|
Cellules nucléées |
5000/mm3 |
100 000/mm3 |
Décès par éclatement de la rate. Le sang périphérique est envahi par les érythroblastes.
Une cellule infectée est une cellule produisant des virus. Une cellule cible est une cellule transformée entraînant une leucémie. Seule la lignée érythroïde est transformée : cible = BFU-E ou CFU-E
Il y a prolifération et différenciation de ces cellules sans EPO. La multiplication anormale de BFU-E et CFU-E entraîne une prolifération des érythroblastes et des globules rouges donc une augmentation de l’hématocrite.
Les gènes env :
Il y a délétion dans la zone de clivage de gp70 et p15E ce qui entraîne la production de gp55 qui a deux propriétés :
- la gp55 se fixe dans la membrane de la cellule infectée donc celle-ci exprime à sa surface gp55 (10% de la gp55 en fait ; 90% reste dans le cytoplasme)
- la gp55 interagit avec le récepteur à l’EPO mais pas sur le même site que l’EPO ; il y a rapprochement des chaînes intra cytoplasmiques ce qui entraîne l’activation. Cette activation est un peu différente de l’activation normale : la voie JAK-STAT au repos. Il y a une activation constitutive (= sans être lié au ligand) de PKàMAPK entraînant la prolifération et de PI3KàAKT entraînant la survie.
· Les étapes de l’érythroleucémie aiguë de Friend
Découverte par Charlotte Friend : la greffe de fragments de rate en fin de maladie sur des souris immunodéficientes (irradiées) provoque une tumeur. Si la greffe est pratiquée en début de maladie il n’y a pas de tumeur. Il s’agit donc d’une maladie multi étapes.
Première étape
BFU-E et CFU-E prolifèrent ; il y a polyclonalité.
Cette première étape se traduit par une prolifération de cellules proérythroblastiques provoquant une hépatosplénomégalie. Ces cellules ne sont pas tumorales car, réimplantées dans une autre organisme, elles ne provoquent pas de tumeurs. Cette première étape de la maladie résulte de l'activation du récepteur à l'EPO.Deuxième étape
Apparition de cellules tumorales pour lesquelles on observe une perte d'activité du gène suppresseur de tumeur P53 et une surexpression d'un facteur de transcription Spi-1 intervenant comme inhibiteur de la différenciation .
Parmi ces cellules une seule prolifère et provoque une tumeur. Cette cellule est la cellule tumorale de Friend (blocage de la différenciation) ; elle est à l’origine d’une lignée monoclonale.
Émergence du caractère tumoral :
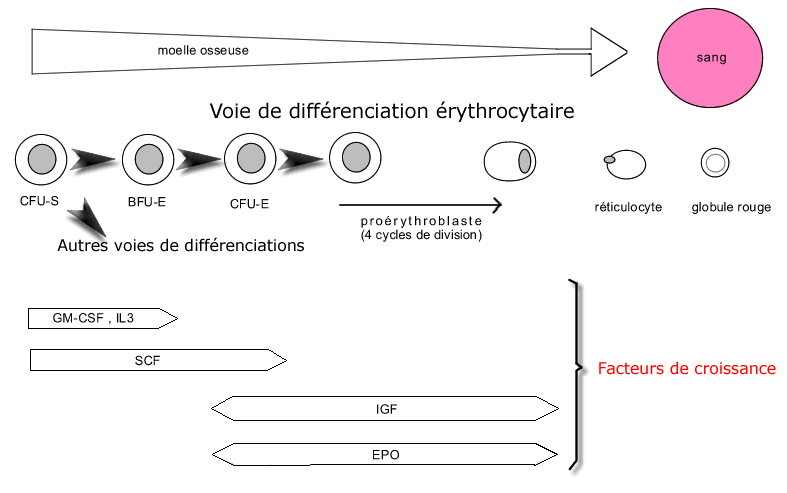
L'analyse de cellules tumorales de différentes souris infectées par le virus SFFV a permis de mettre en évidence l'implication du locus Spi-1 du chromosome 7 dans l'apparition de la maladie de Friend et donc du phénotype tumoral. En effet, on retrouve le même site d'insertion du provirus SFFV chez les différentes souris malades étudiées.
La construction d'une banque d'ADN à partir de tissus infectés, l'identification d'une zone d'insertion du provirus SFFV et l'utilisation de sondes spécifiques de cette zone, a permis de retrouver chez différentes souris développant une maladie de Friend le même site d'insertion viral. Ce site dont la modification est à l'origine du phénotype tumoral est l'oncogène Spi-1.
On parle de mutagénèse insertionnelle :
- insertion dans un exon à extinction du gène
-
insertion dans un promoteur en aval à promotion de l’aval (protéine de fusion)
- insertion en amont ou en aval à activation de la transcription ; les LTR attirent les facteurs de transcription
Mise en évidence d’une intégration provirale :
L'analyse des cellules tumorales d'une même souris infectée a mis en évidence le caractère monoclonal des différentes cellules tumorales ainsi que leur capacité à se disperser dans l'organisme pour envahir de nouveaux territoires (métastases)
Si l’allèle muté contient un provirus avec un site Bam H1 on devrait obtenir 2 bandes en électrophorèse.
Réarrangements génomiques par mutagenèse d’insertion due au SFFV
-
pour détecter une bande en Southern Blot il faut que la population de cellules soit homogène.
-
Les différences de taille en Southern Blot résultent d’insertion différentes à l’intérieur d’un même site.
Le virus SFFV s’insère dans la région génomique courte en amont d’un gène à 5 exons : Spi 1
Il y a alors surexpression d’un messager et de la protéine Spi 1 (55kD)
La protéine Spi1 est un facteur d’activation de la lignée lymphoïde B et de la genèse des macrophages (lignée myelo-monocytaire)
Elle possède deux domaines :
-
un domaine de transactivation : interagit avec la polymerase II et facteur de transcription
-
un domaine de liaison à l’ADN : domaine ETS ; enchaînement d’hélices α et de feuillets β ; le domaine de reconnaissance de l’ADN (85 aa) se lie à un motif riche en purine avec un élément central GGAA et riche en A en amont (voir liste des gènes cibles de Spi 1 dans l’hématopoïèse normale ; Spi 1 = Pu 1 dans l’hématopoïèse normale)
Inactivation de p53 (=facteur de transcription)
-
mutation ponctuelle : dans 5 endroits particuliers (hot spots) ; pour Friend dans le domaine de liaison à l’ADN (3 des hot spots)
-
délétion allélique : fonction normale = gardien du génome
|
La cellule tumorale de Friend = mutagenèse insertionnelle Spi 1 + extinction de p53 + activation du récepteur à l’EPO.
|
· Souris transgénique Spi 1 :
1ère étape : hépato-splénomégalie et anémie (hématocrite 20 à 25 %)
P53 normale
2ème étape