Application pédagogique
Démarche globale
- Le premier point est d’introduire la notion de rétrovirus endogène, c'est-à-dire la présence dans le génome de toutes les cellules de l’organisme et notamment des cellules germinales, de séquences d’origine virale. Pour cela on peut s’appuyer sur l’exemple du rétrovirus endogène KoRV présent chez le Koala.
- Le deuxième point est de mettre en évidence la présence dans le génome humain de gènes codant pour des protéines jouant un rôle physiologique essentiel et d’origine virale. C’est le cas de deux gènes codant pour des syncytines, protéines exprimées dans le placenta embryonnaire qui sont des gènes Env de rétrovirus.
- A ce stade, on peut introduire les notions de transfert horizontal et de transfert vertical dans les processus de diversification des êtres vivants. L’innovation qu’est l’acquisition de séquences rétrovirales, notamment celle du gène Env, par un primate ancestral, résulte d’un transfert horizontal suite au parasitisme de cellules germinales par un rétrovirus exogène ancestral. Ensuite, ces séquences ont été transmises verticalement de génération en génération chez l’espèce ancestrale de primate puis dans toutes les espèces qui en dérivent.
1 - La notion de rétrovirus endogène
Pour traiter cette question, on dispose :
- d’un texte illustré sur les rétrovirus GALV (gibbon-ape leukaemia virus) et KoRV (Koala rétrovirus) qui appartiennent à la même famille de rétrovirus ;
- des séquences des gènes Gag, Pol et Env de ces virus
L'approche de cette notion nécessite un minimum de connaissances sur les rétrovirus, leur génome et leur cycle, en particulier le fait qu'ils incorporent leur génome dans l'ADN de la cellule parasitée (Provirus). Le virus GALV peut servir de support pour dégager les caractéristiques d'un rétrovirus exogène. C'est la comparaison du rétrovirus KoRV avec le rétrovirus exogène GALV qui va permettre de dégager la notion de rétrovirus endogène. Les questions posées aux élèves peuvent donc être d'établir les caractéristiques communes aux rétrovirus GALV et KoRV, puis les différences, et d'aboutir ainsi à la justification de la conclusion suivant laquelle le virus KoRV est un virus initialement exogène devenu endogène. En conclusion, ils doivent proposer un mécanisme possible sur l'endogénisation du virus.
Les génomes des deux virus sont tous les deux insérés dans l'ADN des cellules parasitées et comprennent les mêmes gènes (Env, Pol et Gag) qui présentent de fortes similitudes.
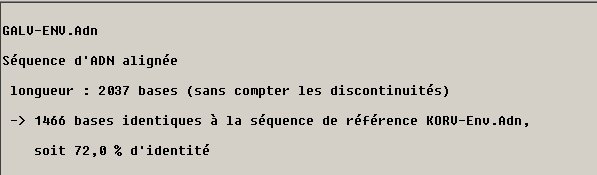
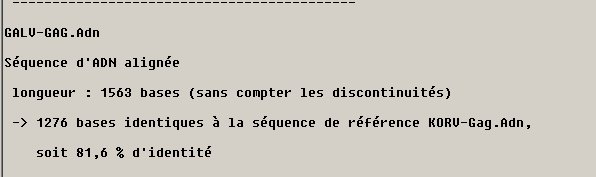

Les différences sont en rapport avec l'information essentielle indiquée dans le texte sur les rétrovirus à savoir que chez beaucoup de Koalas, les séquences provirales de KoRV se trouvent dans toutes les cellules de l'organisme, y compris les cellules germinales, alors que le génome proviral de GALV n'est présent que dans les cellules parasitées. Il en résulte une différence fondamentale sur l'infection des cellules par les deux virus. Dans le cas de GALV, c'est une particule virale qui doit entrer dans une cellule pour la parasiter, alors que dans le cas de KoRV le provirus est présent naturellement dans le génome de toutes les cellules sans infection par un virion exogène. C'est ce qui fait dire que le provirus KoRV est un rétrovirus endogène. Evidemment, des Koalas qui possèdent le provirus endogène peuvent être, en plus, infectés par le virus exogène. On peut donc dire que KoRV est à la fois un rétrovirus exogène et endogène. Cela signifie que KoRV initialement rétrovirus exogène est devenu récemment endogène par un mécanisme d'endogénisation. Certaines populations de Koalas n'ayant pas de provirus endogène KoRV, on peut penser que le processus d'endogénisation n'est pas encore achevé.
Pour faire imaginer ce mécanisme, il est souhaitable de réfléchir à la transmission du génome viral des parents à leur descendance dans le cas des deux rétrovirus GALV et KoRV. Il n'y en a pas dans le cas du provirus GALV. Le virus KoRV, ou plus précisément le provirus KoRV, peut se transmettre de génération en génération car les gamètes des individus parasités possèdent dans leur génome les séquences virales.
A l’origine on doit imaginer une infection de cellules germinales de Koala par le rétrovirus. Le provirus se retrouve dans le génome de la cellule œuf si un gamète le possédant participe à la fécondation. A partir de ce moment, toutes les cellules de l’organisme dérivant de la cellule œuf initiale possèdent une copie du génome viral dans leur ADN. Le provirus intégré fait alors partie du génome de l’organisme : il est devenu endogène. Il continuera d’être transmis verticalement, indépendamment de sa capacité à produire des virions fonctionnels.
2 - La capture de gènes viraux par l’hôte
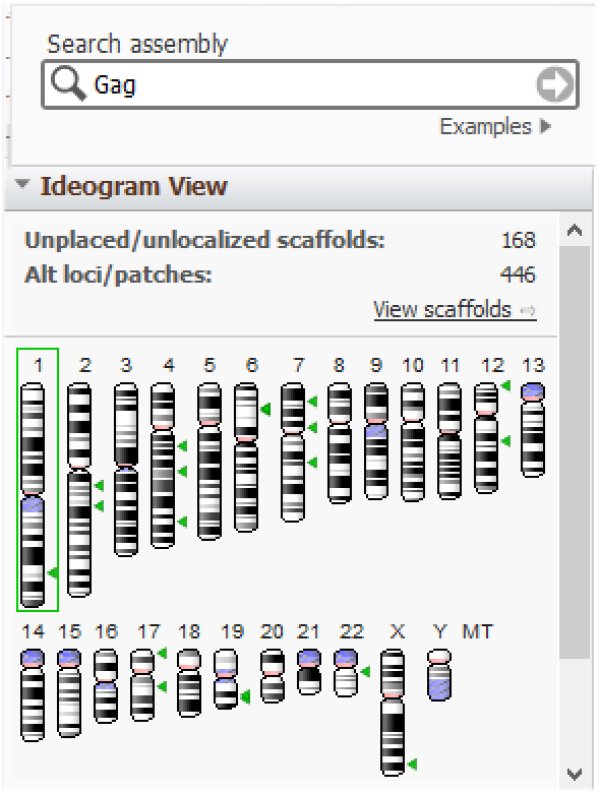
On peut s'interroger sur la présence dans le génome humain de restes de provirus endogènes témoins d'infections passées de cellules germinales d'individus d'espèces ancestrales. Le séquençage complet du génome humain et celui de très nombreux virus ont permis de localiser de tels vestiges. Par exemple, des gènes Env de virus se retrouvent sur de multiples chromosomes :
https://www.ncbi.nlm.nih.gov/genome/gdv/browser/genome/?id=GCF_000001405.39
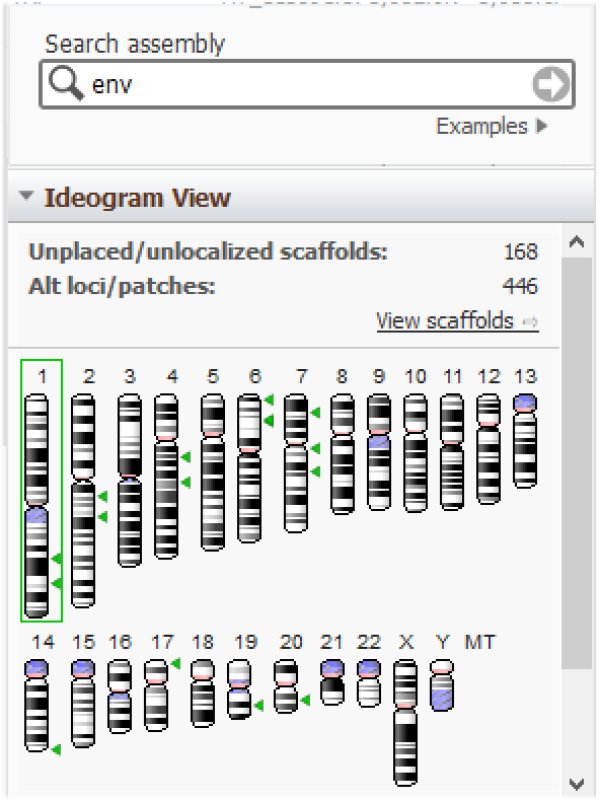
Il en est de même des gènes Gag :
et Pol :
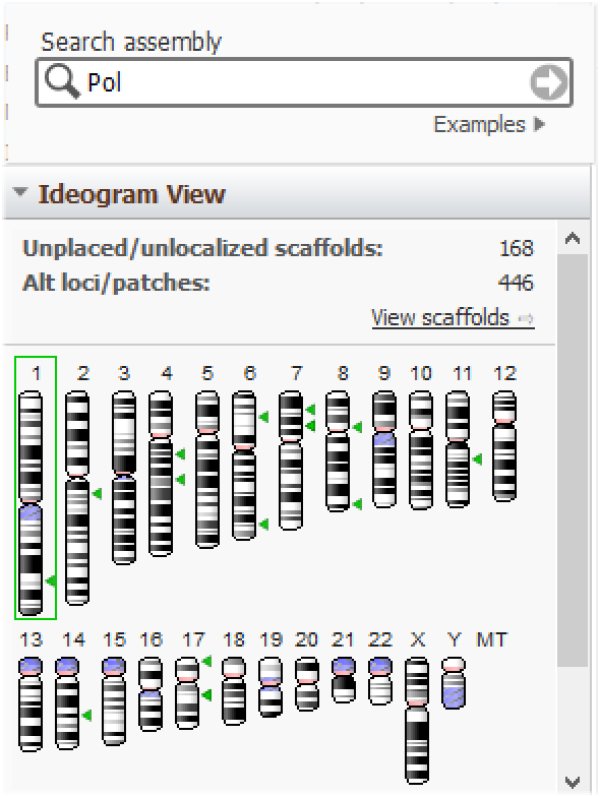
Il n'existe pas de provirus endogènes infectieux chez l'homme. Cela est dû aux mutations ponctuelles et délétions que les gènes viraux ont subies au cours de l'histoire évolutive des espèces qui les ont hébergés.
Cependant, s'il n'existe pas de provirus endogène complet fonctionnel, certains gènes, en particulier les gènes Env, sont encore actifs chez l'homme. C'est le cas de deux gènes HERWE1, situé sur le chromosome 7, et du gène ERV-FRD1 situé sur le chromosome 6. Ces deux gènes codent pour des protéines appelées respectivement syncytine 1 et syncytine 2 et s'expriment uniquement dans le placenta, en particulier au début de sa formation.
Pour aborder ce point, on dispose :
- d’un texte de présentation des Syncytines qui précise la fonction de ces protéines ;
- de la séquence des gènes qui codent pour les syncytines 1 et 2 et du gène Env d’un rétrovirus MSRV (Multiple sclerosis-associated retrovirus), qui a été trouvé chez des personnes atteintes de sclérose en plaque.
On peut demander aux élèves d'exploiter ces documents et séquences afin de montrer en quoi ils confirment l'idée que le gène codant pour la syncytine 1 est d'origine virale.
La comparaison avec Anagène de la séquence de syncytine 1 avec celle de la protéine du rétrovirus exogène MSRV révèle une similitude de 87%. Cette forte similitude corrobore l'idée que la syncytine 1 est d'origine virale. Celle-ci est aussi confirmée par la similitude des fonctions de la syncytine 1 et de la protéine d'enveloppe du virus : toutes les deux sont des protéines fusiogènes. La protéine virale permet la fusion de l'enveloppe virale avec la membrane cellulaire, et donc l'entrée du virus dans la cellule. La Syncytine1 permet la fusion des membranes des cellules du trophoblaste qui devient une couche multinucléée, le syncytiotrophoblaste, étape indispensable à l'élaboration du placenta.
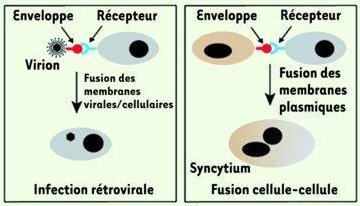
Similitude des fonctions de la protéine d'enveloppe d'un rétrovirus exogène à gauche et des syncytines 1 et 2 à droite. D'après Médecine/science 2011, N° 27, A. Dupressoir et T. Heidmann.
Remarque : la comparaison de la séquence de la syncytine 2 avec celle de la protéine d'enveloppe du MSRV révèle une similitude assez faible (de l'ordre de 22%). Cela n'infirme pas cependant l'idée que la syncytine 2 est d'origine rétrovirale. En effet, les gènes Env des rétrovirus exogène actuels ont des séquences de leurs protéines d'enveloppe très variables (il existe de multiples familles de rétrovirus). Toutes ces protéines d'enveloppe sont des protéines à propriétés fusiogènes mais elles diffèrent dans leur spécificité de reconnaissance des récepteurs auxquels elles se lient. Le gène de la syncytine 2 a donc pour origine une infection de cellules germinales d'un primate ancestral par un rétrovirus différent de celui à l'origine de la syncytine 1.
3 - Datation de l'infection par les rétrovirus à l'origine des Syncytines 1 et 2
On a recherché des gènes homologues des syncytines 1 et 2 chez divers primates. On peut demander aux élèves d'exploiter les fichiers de séquences pour essayer de dater le moment où s'est faite l'intégration dans le génome des gènes à l'origine des syncytines 1 et 2 et de reporter leurs conclusions sur un arbre phylogénétique des Primates.
Cet exercice a l'intérêt d'entraîner à placer une innovation évolutive sur un arbre phylogénétique existant. Ainsi, si tous les Hominoïdes possèdent le gène de la syncytine 1 alors que les autres primates ne le possèdent pas, c'est que l'infection rétrovirale à l'origine de la syncytine 1 a eu lieu dans la branche menant aux Hominoïdes après sa séparation avec celle qui mène aux Cercopithèques (Macaque, Babouin, etc.). Les élèves devraient ainsi aboutir au schéma suivant :

D'après Médecine/science 2011, N° 27, A. Dupressoir et T. Heidmann.
Remarque : Le raisonnement précédent suppose que l'on fournisse aux élèves un arbre phylogénétique des Primates. Cet arbre est de toute façon envisagé dans la partie du programme relative à l'évolution humaine. Il est donc possible de le faire construire au préalable à partir des données de Phylogène.
Il est même possible d'ébaucher cet arbre à partir des données sur les syncytines en utilisant le raisonnement habituel sur les données moléculaires pour établir les relations de parenté.
Conclusion : transfert horizontal et transfert vertical
L’incorporation d’un rétrovirus dans le génome d’une espèce résulte d’un transfert horizontal. En revanche la transmission du provirus au cours des générations successives d’une espèce, puis de celles qui en dérivent, résulte d’un transfert vertical classique.
Cette étude sur la présence de gènes rétroviraux dans le génome des mammifères révèle l'importance du transfert horizontal dans les processus de diversification du vivant.