Evolution des motoneurones en culture
Ecrit par Jean-Pierre Ternaux
ACTIVITE ELECTRIQUE DES MOTONEURONES EN CULTURE
La maturation morphologique des motoneurones purifiés maintenus en culture s'accompagne d'une maturation des propriétés fonctionnelles de ces neurones.
L'activité électrophysiologique des motoneurones peut être enregistrée en utilisant les techniques de patch clamp en configuration "cellule entière".
Les lamelles de culture sont transférées dans une chambre de perfusion sur la platine d'un microscope inversé. Une électrode de patch est descendue sous contrôle microscopique jusqu'à la surface membranaire du corps cellulaire du motoneurone.
Le patch est réalisé par aspiration à l'aide d'une seringue.
Les signaux électriques obtenus (potentiels d'action et potentiels synaptiques, dans le cas de culture plus âgées) sont amplifiés et enregistrés .
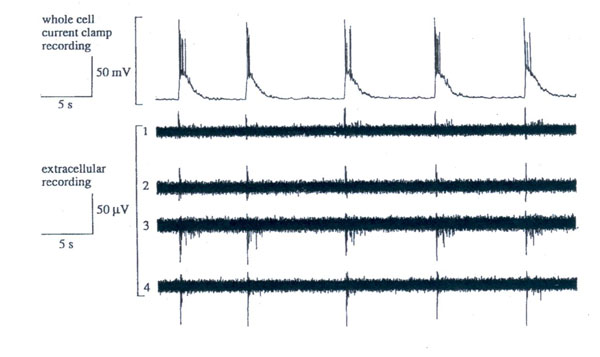 |
| Activité electrique des motoneurones spinaux en culture: Culture de motoneurones purifiés maintenue pendant 13 jours. Enregistrement à l’aide d’une électrode de patch clamp de l’activité spontanée des motoneurones. Les enregistrement effectués sur les pistes 1, 2, 3 et 4 correspondent à des enregistrements extracellulaires avec des électrodes placées dans différentes régions de la culture (enregistrement à distance dans le réseau de neurones formé en culture). Les décharges du motoneurone enregistrées en configuration « cellule entière » se présentent sous forme de bouffées de plusieurs potentiels d’action. (d’après Yasuhiko Jimbo et Jean-Pierre Ternaux) |
QUANTIFICATION DES EFFETS DE DIFFERENTES SUBSTANCES
-
QUANTIFICATION DE LA SURVIE DES MOTONEURONES EN CULTURE
La survie des motoneurones peut être quantifiée à chaque étape du développement en culture et l’effet de différentes substances additionnées au milieu de culture (facteurs neurotrophiques, neurotransmetteurs, etc...) ou l’ajout d’inserts contenant des types cellulaires différents (cellules gliales et interneurones, myoblastes embryonnaires, etc ...) peut être évalué.
Chaque jour, dans des cultures contrôles (en présence de milieu « défini ») ou dans des cultures traitées, 12 champs microscopiques, sélectionnés au hasard, sont photographiés (grossissement : x 150) sur chaque lamelle de culture.
Le nombre de motoneurones présent est déterminé par comptage.
La moyenne du nombre de motoneurones est exprimée en pourcentage du nombre de motoneurones déterminé avec la même méthode, une heure après la mise en culture. L’évolution temporelle de la survie des motoneurones peut être comparée dans les conditions contrôles (milieu « défini ») et lors de l’ajout de diverses substances ou de type cellulaires différents.
Dans ces conditions, il est possible de déterminer, par exemple, si une molécule X possède des effets neurotrophiques sur le développement du motoneurone embryonnaire.
-
ANALYSE STATISTIQUE MORPHOMETRIQUE QUANTITATIVE DES MOTONEURONES EN CULTURE
Pour analyser et quantifier la maturation et la différentiation morphologique des motoneurones maintenus en culture et pour évaluer les effets de différentes substances pharmacologiques ou de différents types cellulaires ajoutés dans ces cultures, plusieurs paramètres morphologiques pertinents peuvent être mesurés à chaque étape du développement.
Ainsi, chaque jour, 50 motoneurones, sélectionnés au hasard dans les cultures contrôles et les cultures témoins, sont photographiés.
A partir des documents issus de l’imprimante vidéo, il est possible en utilisant une tablette graphique et un logiciel de morphométrie, de mesurer, pour chaque motoneurone, les paramètres suivants :
- le nombre de neurites primaires émergeant du corps cellulaire,
- le nombre de bifurcations totales sur l’ensemble de l’arborisation neuritique,
- le nombre de bifurcations par neurite,
- la longueur totale des neurites,
- la longueur de l’axone (pour le motoneurone il s’agit dans tous les cas de la plus longue neurite, ceci est confirmé en immunohistochimie par le marquage avec un anti MAP spécifique des axones),
- la longueur des dendrites.
Le logiciel utilisé permet de tracer un polygone convexe dont les sommets passent par l’extrémité des différentes neurites et d’en calculer la surface.
Cette surface correspond à une surface d’étalement du neurone sur son substrat.
Elle peut varier en fonction des molécules mises en présence des motoneurones en culture.
En utilisant cette mesure de surface du polygone d’étalement du neurone et en mesurant la plus longue diagonale de ce polygone irrégulier, il est possible de calculer l’index d’étirement du neurone observé qui constitue un index morphologique particulièrement intéressant à analyser dans différentes situations expérimentales. Cet index est calculé en utilisant la formule suivante : IE = p d2 / 4 S, où d est la plus longue diagonale et S la surface du polygone.
Pour chaque paramètre étudié et pour chaque stade du développement, on calcule la moyenne et l’erreur standard à la moyenne des 50 motoneurones analysés.
Les résultats obtenus dans les conditions contrôles ou en présence de différentes substances sont statistiquement comparés en utilisant un test t de Student .
 |
|
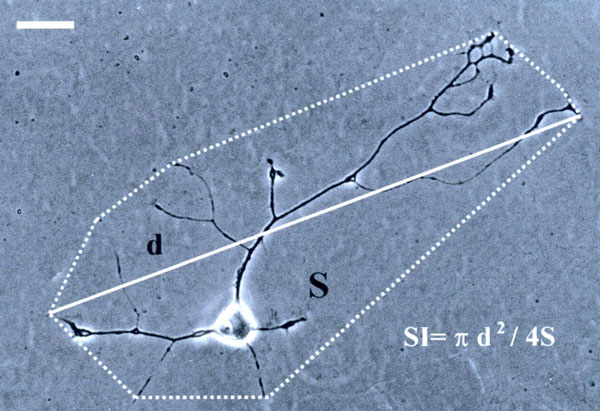
Analyse statistique quantitative morphométrique
Chaque jour 50 à 60 motoneurones sont sélectionnés au hasard dans les cultures. Les paramètres morphologiques suivant sont mesurés : -le nombre de neurites primaires émergeant du corps cellulaire -le nombre de bifurcations -la longueur totale des neurites -la longueur de l’axone -la longueur des dendrites -la surface d’étalement du neurone : surface du polygone convexe passant par l’extrémité des neurites -l’index d’étirement correspondant à la formule IE= pd2 / 4S ou correspond à la plus longue diagonale du polygone convexe et S la surface d’étalement. Les résultats sont exprimés en valeur moyenne ± l’erreur standard. Echelle : 20 µm. |
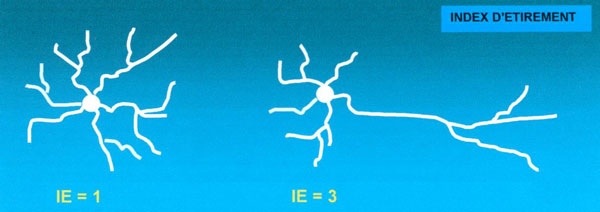 |
| Exemples de valeurs d'index d'étirement IE, en fonction de la forme du motoneurone |