litho_point1
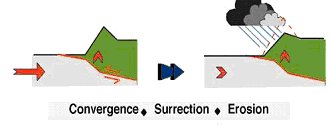
L'impact de l'altération des roches sur la quantité de carbone atmosphérique.
Altération des carbonates | Altération des silicates | ||
Soumis aux pluies acides, les carbonates sont très vite attaqués : CaCO3 + H2O +CO2 ----- Ca2+ + 2HCO3- (1) Cette réaction d'altération des carbonates de calcium est celle que l'on trouve dans tous les ouvrages de références. Si on l'analyse on constate que l'altération des carbonates donne 2HCO3- : un est issu du CO2 atm et l'autre du minéral. De manière instantanée on a bien consommation d'un CO2 de l'atmosphère.
Que deviennent ces deux HCO3-formés ? Transportés par les eaux de ruissellement puis les fleuves ils se retrouvent dans l'océan. Il est de même pour le Ca2+ qui a été libéré simultanément (1). Dans l'océan le Ca2+ arrivant est une manne pour les organismes à coquille et test calcaires qui l'utilisent grâce l'anhydrase carbonique selon la réaction :
Ca2+ + 2HCO3- ----- CO2 + H20 + CaCO3(2) Ceci à deux conséquences : - Augmentation de la [] ° en CO2 - Consommation de HCO3- L'augmentation de CO2 entraîne un gradient entre l'océan et l'atmosphère qui favorise la diffusion du CO2vers l'atm. Cette diffusion compense la soustraction d'un CO2 à l'atmosphère lors de l'altération. (1) L’augmentation de CO2 entraîne un gradient entre l’océan et l’atmosphère qui favorise la diffusion du CO2 vers l’atm. (véritable réaction chimique contrôlée par la loi de Henry)
Cette diffusion compense la soustraction d’un CO2 à l’atmosphère lors de l’altération. (1) Bilan : Le cycle altération/précipitation des carbonates donne au final un bilan nul pour les variations de CO2. En d’autre terme, l’altération des carbonates puisqu’elle est compensée par une précipitation océanique ne consomme pas « réellement » de CO2. |
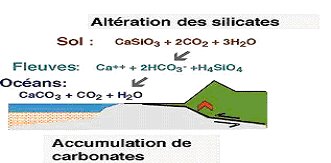
La littérature abonde dans le sens d'une consommation de CO2 atm par l'altération. C'est dans l'altération des silicates que cette affirmation trouve son sens.
Exemple de l'anorthite (plagioclase Ca) : CaAl2Si2O8 + 3H2O + 2C02 ---- Ca2+ + kaolinite + 2HCO3- (3) Dans cette réaction on note la fixation de deux CO2 d'origine atmosphérique. Que deviennent ces deux HCO3- formés ? Les deux HCO3- (origine atmosphérique) sont acheminés par l'eau douce vers l'océan. Accompagnés de Ca2+, un des deux participe à la formation CaCO3 et l'autre est restitué à l'atm (2).
Bilan : Seule l'altération des silicates consomme " réellement " du CO2 atmosphérique grâce à un stockage au sein des carbonates.
Images issues du site du CNRS.
|
LE MECANISME EST TOUJOURS OPERANT AUJOURD’HUI. IL SUFFIT DE CONSTATER QUE LA QUANTITÉ DE CO2 CONSOMMEE PAR ALTERATION DES SILICATES AUJOURD' HUI EGALE A PEU PRES LA QUANTITE DE CARBONE INCORPOREE DANS LES CARBONATES QUI PRECIPITENT DANS L’OCEAN.