moment dipolaire
Par Christelle LANGRAND
—
Dernière modification
19/09/2017 09:51
Définition du moment dipolaire
Un dipôle électrique est constitué de deux charges électriques opposées (+q et -q) placées à une distance d l'une de l'autre. Il est caractérisé par son moment dipolaire c'est à dire un vecteur colinéaire à la liaison, orienté de la charge négative vers la charge positive, de norme μ = q*d exprimée en debye (1D = 3,33.10-30 C.m-1)
Définition d'une molécule à caractère dipolaire
Une molécule est une entité neutre constituée d'atomes reliés entre eux par des liaisons covalentes. Chaque atome est caractérisé par son électronégativité c'est-à-dire sa capacité à attirer plus ou moins les électrons des liaisons qu'il forme avec un autre atome au sein de la molécule. Ainsi, l'atome d'oxygène est plus électronégatif que l'atome de carbone dont l'électronégativité très légèrement supérieure à celle de l'atome d'hydrogène. On peut alors assimiler les atomes à des "charges" positives ou négatives.
Une molécule est dite à caractère dipolaire lorsque le barycentre de ses "charges" positives ne coïncide pas avec celui de ses "charges" négatives.
Exemple: la molécule d'eau a un caractère dipolaire
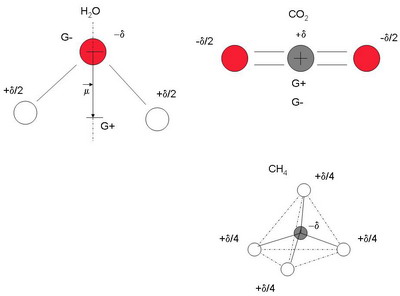
Les deux atomes d'hydrogène sont "chargés" +δ/2. Comme le montre le schéma ci-dessous, leur barycentre se trouve sur l'axe de symétrie de la molécule.
L'atome d'oxygène est chargé -δ et son centre est confondu avec le barycentre de la "charge" négative.
Comme les deux barycentres ne coïncident pas, la molécule d'eau est donc un dipôle électrique et est caractérisée par son moment dipolaire.
Exemples: les molécules de dioxyde de carbone (CO2) et de méthane (CH4) ne sont pas des dipôles (schéma ci-dessous)
La molécule de dioxyde de carbone est linéaire et symétrique par rapport à l'atome de carbone. Les atomes d'oxygène sont "chargés" -δ/2 et leur barycentre est confondu avec le centre de l'atome de carbone chargé +δ. Les barycentres coïncident; cette molécule n'a donc pas de caractère dipolaire.
La molécule de méthane est tétraédrique. Les quatre atomes d'hydrogène portent chacun une "charge" très faible notée +δ/4; leur barycentre est confondu avec le centre de l'atome de carbone qui est échargé" -δ. Dans ce cas, les deux barycentres coïncident et la molécule de méthane n'a donc pas de caractère dipolaire.
Une molécule est dite à caractère dipolaire lorsque le barycentre de ses "charges" positives ne coïncide pas avec celui de ses "charges" négatives.
Exemple: la molécule d'eau a un caractère dipolaire
Les deux atomes d'hydrogène sont "chargés" +δ/2. Comme le montre le schéma ci-dessous, leur barycentre se trouve sur l'axe de symétrie de la molécule.
L'atome d'oxygène est chargé -δ et son centre est confondu avec le barycentre de la "charge" négative.
Comme les deux barycentres ne coïncident pas, la molécule d'eau est donc un dipôle électrique et est caractérisée par son moment dipolaire.
Exemples: les molécules de dioxyde de carbone (CO2) et de méthane (CH4) ne sont pas des dipôles (schéma ci-dessous)
La molécule de dioxyde de carbone est linéaire et symétrique par rapport à l'atome de carbone. Les atomes d'oxygène sont "chargés" -δ/2 et leur barycentre est confondu avec le centre de l'atome de carbone chargé +δ. Les barycentres coïncident; cette molécule n'a donc pas de caractère dipolaire.
La molécule de méthane est tétraédrique. Les quatre atomes d'hydrogène portent chacun une "charge" très faible notée +δ/4; leur barycentre est confondu avec le centre de l'atome de carbone qui est échargé" -δ. Dans ce cas, les deux barycentres coïncident et la molécule de méthane n'a donc pas de caractère dipolaire.