Proposition 3 - Les notions de gènes suppresseurs de tumeurs
3 - Les notions de gènes suppresseurs de tumeurs
La lecture de ces deux documents sensibilisent à l’idée de l’existence au sein des cellules normales d’un mécanisme génétique qui s’oppose à leur cancérisation.
Le gène P53 est un des principaux gènes en jeu. Son action peut être analysée à partir des documents suivants :
« Données expérimentales chez la souris »
et
« Les informations fournies par l’analyse de données génétiques chez l’Homme »
Le premier document révèle qu’en l’absence d’allèle P53, les souris ont une fréquence élevée de tumeurs qui apparaissent de manière précoce. Cela indique que les allèles P53 des cellules s’opposent normalement à la cancérisation, ce qu’on traduit par gène suppresseur de tumeur, terme un peu ambigu. Il veut dire seulement que la protéine codée par le gène bloque l’entrée de la cellule dans un processus cancéreux.
Le deuxième document repose sur l’arbre généalogique d’une famille où plusieurs membres sont atteints d’une tumeur à un jeune âge (syndrome de Li-Fraumeni) pouvant atteindre des organes divers. Il s’agit donc d’un cas de cancer héréditaire ou plus précisément de prédisposition à développer une tumeur. L’analyse de l’arbre révèle l’implication du gène P53 dans la genèse des tumeurs car les sujets atteints ont deux allèles mutés P53 dans leurs cellules cancéreuses. Un allèle provient d’un des parents et l’autre résulte d’une mutation somatique du deuxième allèle normal dans une cellule. L’expérience de transfection indique que l’allèle normal limite nettement la prolifération de cellules cancéreuses en culture, ce qui n’est pas le cas de l’allèle muté. Cela confirme le statut de gène suppresseur de tumeur de P53.
1 – Les informations fournies par le modèle souris
Les élèves doivent d’abord bien saisir que le protocole expérimental utilisé fait que toutes les cellules de la souris ont le même génotype de sorte qu’en comparant les trois classes de souris, on va étudier l’influence de la perte de fonction d'un ou de deux allèles P53 sur la cancérisation des cellules.
On constate que dans la première expérimentation avec la lignée C57BL6, près de 100% des souris dépourvues d'allèles fonctionnels du gène P53 (P53-//P53-) sont mortes à 6 mois, alors que la mortalité des souris hétérozygotes (P53+//P53-) ne débute que vers 9 mois, et qu’une seule souris ayant deux allèles P53 fonctionnels est morte durant la durée de l’expérience.
Puisque les souris appartiennent toutes à la même lignée et qu’elles ont été élevées dans les mêmes conditions, on peut en conclure que l’absence de tout allèle fonctionnel du gène P53, si elle n’empêche pas le développement des souris, entraîne néanmoins une mort prématurée. Surtout, plus de 80% des souris de génotype P53-//P53- ont présenté des tumeurs durant leur vie, et très précocement, contre 17% des hétérozygotes (P53+//P53-) et moins de 3% des souris P53+//P53+. On constate aussi que les tumeurs sont apparues plus tardivement chez les hétérozygotes que chez les homozygotes P53-//P53-.
On peut donc en conclure que l’absence de tout allèle fonctionnel du gène P53 favorise l’apparition des tumeurs. Puisqu’une tumeur a pour origine une seule cellule, cela signifie que l’absence d’allèle P53 fonctionnel a pour effet d’augmenter la probabilité pour une cellule de devenir cancéreuse.
Le pourcentage de souris hétérozygotes P53+//P53- développant des tumeurs est plus important que celui des souris de génotype normal. L’absence d’un seul allèle fonctionnel prédispose donc les cellules à devenir cancéreuses, même si cette prédisposition est inférieure à celle constatée en l’absence de tout allèle P53 fonctionnel.
Puisque l’absence d’un allèle P53 normal, et encore plus celle de 2 allèles normaux, prédispose fortement à l’apparition de tumeurs, cela signifie que chez les animaux P53+//P53+ élevés dans les mêmes conditions, les allèles P53 normaux s’opposent à la cancérisation des cellules. Cela est une caractéristique d’un gène suppresseur de tumeur. Il faut garder à l'esprit que la cellule est soumise à des facteurs internes ou externes qui tendent à provoquer sa cancérisation, et que le rôle de P53 est de s'y opposer en permanence.
La deuxième expérimentation avec la deuxième lignée de souris débouche globalement sur les mêmes constats et donc les mêmes conclusions sur la fonction suppresseur de tumeur du gène P53. Toutefois, on constate que les hétérozygotes de cette lignée développent plus rapidement et fréquemment des tumeurs que ceux de la première expérimentation. Cela indique que la fonction de P53 dépend d'autres caractéristiques génétiques et suggère que le gène P53 n’est pas le seul en cause dans la cancérisation.
2 - Les informations fournies par l’analyse d’un arbre généalogique dans l’espèce humaine
Un cas de cancer héréditaire
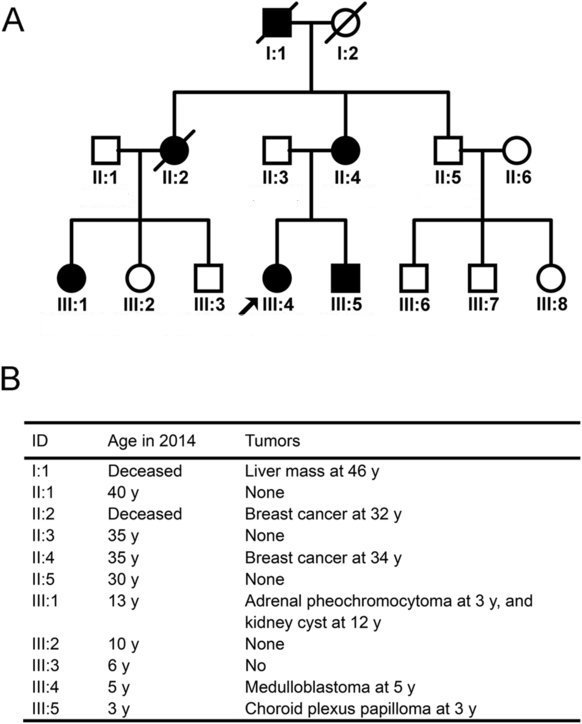
On constate des cas de cancer dans cette famille sur trois générations. En outre, ces cancers sont précoces par rapport à l’apparition des cancers dans la population générale : 3 , 5 et 12 ans pour les enfants de la troisième génération, 32 et 34 ans pour les personnes de la deuxième génération, 46 ans pour l’homme de la première génération. On constate également la diversité des cancers dans la famille : cancer du foie, cancer du sein, cancer du cerveau, du rein. Ces informations laissent à penser que le cancer est héréditaire dans la famille (au sens courant du terme).
Un cancer héréditaire où le gène P53 est en cause
La détermination des génotypes des membres de la famille réalisée par les cliniciens permet de savoir si le gène P53 peut être en cause et tester l’idée de cancer héréditaire.
