Commentaire-1 - Système immunitaire et cancers
I - Immunité antitumorale
1 - Système immunitaire et cancers
1.1 Rapide historique sur l’évolution des idées
La seconde moitié du 19ème siècle voit la mise en évidence de l’implication de microorganismes pathogènes, bactéries et virus, dans les maladies infectieuses. Des mécanismes de défense de l’organisme contre ces pathogènes, notamment la phagocytose et les anticorps sont découverts. Des traitements préventifs (vaccination, asepsie) et curatifs (sérothérapie, antisepsie) qui découlent de ces connaissances sont mis en oeuvre. Le 20ème siècle ne fera que confirmer et enrichir les mécanismes et les rôles du système immunitaire contre les pathogènes. En revanche, malgré des médecins et immunologistes avant-gardistes, le fait que le système immunitaire ait une action contre les tumeurs cancéreuses a fait l’objet de controverses pendant une grande partie du 20ème siècle. Ce n’est que vers la fin de ce siècle que la communauté scientifique a admis le rôle antitumoral du système héréditaire et que se sont développés au début du 21ème siècle et surtout à partir du début des années 2010 les traitements d’immunothérapie contre les cancers. C’est une évolution importante. Jusque là les traitements par chirurgie, chimiothérapie, radiothérapie étaient ciblés sur les cellules tumorales. Toujours en oeuvre, ces traitement sont complétés par ceux de l’immunothérapie, notamment dans le cas de certains cancers où les traitements classiques n’agissent pas. Avec l’immunothérapie, on agit sur le système immunitaire pour l’activer et faire qu’il devienne efficace contre les cellules tumorales. L’immunothérapie par les cellules CAR-T envisagée dans ce dossier n’est qu’un des traitements d’immunothérapie mis en oeuvre actuellement. Elle a été autorisée par les autorités de santé en 2017 en Amérique et en 2018 en Europe.
1.1.1 William B. Coley et les premières idées sur le rôle antitumoral du système immunitaire et sur l’immunothérapie
William Coley (1862-1936) jeune chirurgien responsable du service des tumeurs osseuses dans un hôpital de New York, a eu comme patiente, en 1890, une jeune femme avec une tumeur osseuse de la main. Elle a subi une amputation de l’avant-bras, mais malgré ce traitement chirurgical, elle est décédée 10 semaines plus tard sans doute à cause de métastases. Profondément affecté par ce décès, Coley consulta les registres de l’hôpital relatant l’histoire d’autres patients. Il a ainsi découvert le cas d’un patient atteint, 7 ans auparavant, d’une tumeur osseuse inopérable chez qui les médecins avaient constaté une régression de la tumeur à la suite d’une infection bactérienne causée par des streptocoques. Coley réussit à retrouver ce patient et constata que sa tumeur avait disparu. Il décida alors d’étudier la littérature scientifique sur les traitements de tumeur osseuse et a ainsi découvert l’existence d’autres cas de régression de la tumeur suite à des infections microbiennes.
Coley était au courant des connaissances en immunologie de l’époque et donc du rôle du système immunitaire contre les microbes. Pour comprendre l’évolution différente du cancer chez sa patiente décédée et les cas de régression de la tumeur suite à une infection, il a fait l’hypothèse que les infections bactériennes chez ces patients étaient à l’origine de la régression tumorale. Le système immunitaire avait réagi contre elles et cette réponse immunitaire non spécifique avait eu aussi une action destructrice sur les cellules tumorales.
C’est la première fois qu’a été émise l’hypothèse du rôle antitumoral du système immunitaire.
Préoccupé par la nécessité de trouver des traitements autres que chirurgicaux, Coley en 1891, injecta à un patient atteint d’une tumeur incurable une suspension de streptocoques. Elle déclencha une infection avec une forte fièvre mais elle a provoqué une régression importante de la tumeur. Encouragé par ce succès, il répéta le traitement chez d’autres patients et il en publia les résultats dans un article intitulé « The treatment of malignant tumors by repeated inoculations of erysipelas, with un report of ten cases. 1893 ».
L’érysipèle est une infection bactérienne de la peau généralement causée par le streptocoque. Chez 8 de ses patients, la régression de la tumeur inopérable a été nette allant chez certains à la disparition. Deux des patients ont vu une régression de leur tumeur mais ont succombé à leur infection. Coley modifia le produit injecté de façon à limiter le risque d’infection, produit qui a été appelé « les toxines de Coley ». Coley, pendant quarante années traita ainsi plus de 1000 patients atteints de tumeurs osseuses inopérables et d’autres médecins ont utilisé le même traitement thérapeutique. Les résultats ont été divers pour des causes multiples (variations dans le produit injecté, dans la méthode d’administration - injection intraveineuse, directement dans la tumeur). De nombreuses critiques ont été faites à la thérapeutique préconisée par Coley et avec les développements de la chimiothérapie et de la radiothérapie, elle a été abandonnée.
Puisque que dans son principe, elle repose sur l’idée d’une stimulation des défenses de l’organisme pour lutter conte le cancer, elle constitue le premier traitement d’immunothérapie utilisé. C’est pourquoi, Coley est considéré comme le « père de l’immunothérapie ».
Cet historique ne se trouve pas dans les documents du dossier. Il permet une réflexion sur la pratique médicale. Les limites de l’immunothérapie pratiquée par Coley sont dues au fait que les connaissances à cette époque sur le fonctionnement du système immunitaire ne permettaient pas d’expliquer l’efficacité de cette thérapeutique. L’immunothérapie sur les cellules CAR-T envisagée dans la seconde partie de ce dossier repose elle sur les connaissances acquises depuis lors sur le fonctionnement du système immunitaire. C’est une illustration de la connexion entre la science fondamentale et ses applications cliniques qui contribuent elles-mêmes à l’évolution des connaissances.
1.1.2. Réalité de l’action antitumorale du système héréditaire
a - Les conséquences de l’immunodéficience sur les cancers
Les personnes « transplantées » sont immunodéficientes suite au traitement pour éviter le rejet de l’organe reçu. Statistiquement, on a constaté que dans les années qui suivent la transplantation, ces personnes ont une fréquence nettement supérieure à celle de personnes immunocompétentes témoins. Cela indique que le système immunitaire s’oppose à la formation de tumeurs cliniquement décelables donc qu’il a une action antitumorale.
b - L’infiltration lymphocytaire
Les observations cytologiques ont révélé la présence de cellules immunitaires, en particulier de lymphocytes T cytotoxiques au sein des tumeurs, établissant des contacts avec les cellules tumorales. Cela laisse supposer que ces lymphocytes appelés TIL (Tumor infiltrating lymphocytes) exercent une action sur les cellules tumorales.
L’infiltration lymphocytaire présente dans toutes les tumeurs solides, en particulier les mélanomes - cancers cutanés - présente trois phénotypes distinctifs comme l’illustre la figure du document 2. Les différences entre ces phénotypes portent sur l’intensité et la localisation de l’infiltration, absente dans certaines tumeurs, localisée à la périphérie chez d’autres, au sein de la tumeur chez un troisième phénotype. L’observation clinique importante faite dans le cas du mélanome est la corrélation entre le phénotype de la tumeur et la survie des patients. Les patients ayant une tumeur de phénotype « inflamed » avec une forte infiltration lymphocytaire, ont une survie plus grande que ceux ayant un des deux autres phénotypes. Cela confirme l’hypothèse de l’action anti cellules tumorales des lymphocytes T effecteurs et donc du système immunitaire.
c - Confirmation de l’action antitumorale des TILs
Dans la seconde moitié des années 1980, l’équipe de Rosenberg réalisa une immunothérapie cellulaire adoptive par transfert de TIL à des patients atteints d’un cancer, précisément d’un mélanome avec métastases pour lequel la chimiothérapie et la radiothérapie étaient inefficaces. Le protocole suivi est illustré par la figure ci-dessous.
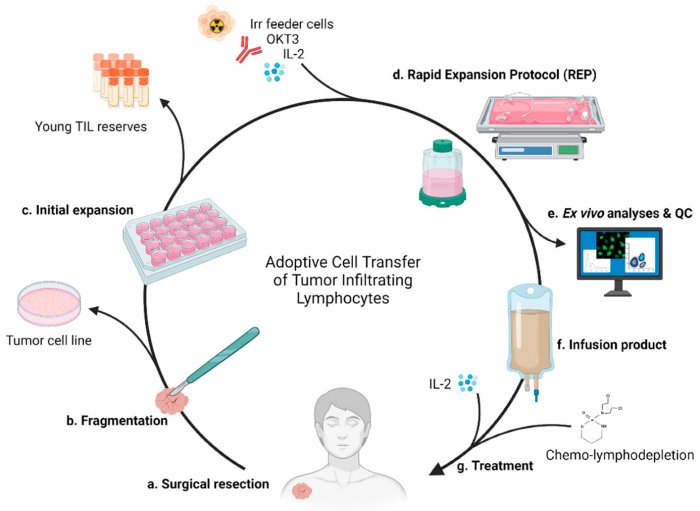
Source : Thomas Morgan Hulen et al. ACT up Til now The evolution of TIls in adoptive cell trherapy for the treatment of solid tumors. MDPI. 9 July 2021.
Légendes
a. Résection chirurgicale : La résection d’au moins 1 à 2 cm de diamètre de la tumeur est la première étape du processus.
b. Fragmentation : l’échantillon de tumeur recueilli est scindé en fragments de 1 à 3 mm qui sont disposés sur des milieux de culture et les lymphocytes séparés des cellules tumorales.
c. Expansion initiale des TIL stimulée par l’interleukine 2, cytokine produite par génie génétique. Les lymphocytes peuvent être cryo préservés en attente de la planification du traitement.
d. Les lymphocytes sont placés dans un système automatisé de culture cellulaire permettant une expansion rimportante.
e. Analyse ex vivo du produit : des tests visant à certifier la stérilité et l’absence de cellules tumorales sont effectués.
f. Avant le traitement proprement dit, une chimiothérapie de 5 à 7 jours ayant pour objectif de provoquer une déplétion des lymphocytes est réalisée. Elle évite une compétition entre les lymphocytes T endogènes et les TILs. Elle permet de générer un environnement favorable aux TILs et favorise leur infiltration dans la tumeur.
g. Réinfusions des TILs chez le patient : le nombre de TILs injectés est compris entre 1.10 puissance 9 et 1.10 puissance 11. Des perfusions de l’IL2 sont effectuées afin de faciliter la prolifération des TILs injectés chez le patient, et leur pérennisation.
Dans un rapport préliminaire de 1988, Rosenberg et son équipe rapportent les résultats du premier essai clinique d’une immunothérapie réalisée par transfert de TILs. Ils ont traité 20 patients atteints d’un mélanome métastasé suivant un protocole proche de celui illustré par la figure. Chez 11 patients, ils ont constaté une régression de la tumeur de la peau, des poumons, du foie, des os, régression qui a persisté de 2 à 13 mois.
Ils précisent que le peu de recul de leur essai clinique fait qu’il est trop tôt pour savoir si cette forme d’immunothérapie peut améliorer la survie des patients. De nombreuses équipes ont par la suite utilisé cette technologie notamment lorsque la tumeur est réfractaire à la chimiothérapie et à la radiothérapie. Pour ne citer qu’un seul exemple, on peut prendre celui de Michal J. Besser et son équipe qui, dans un article publié en 2010 (Clinical responses in a phase II study using adoptive transfer of short-term cultured tumor infiltration lymphocytes in metastatic melanoma patients), rapportent avoir traité 20 patients atteints d’un mélanome avec des métastases suivant le même principe que celui de Rozenberg, mais avec quelques modifications. Ils ont constaté une régression objective des tumeurs chez 10 patients avec deux d’entre eux en rémission complète (20 mois et 4 mois après l’immunothérapie). Ces 10 patients étaient tous vivants au moment de l’écriture de l’article (18,13, 10, 9, 6, 4, 3, 3 mois après avoir reçu le traitement).
L’immunothérapie de Coley avait sensibilisé au rôle possible des défenses immunitaires de l’organisme sur les tumeurs cancéreuses, mais faute de connaissances sur les mécanismes immunitaires, elle n’a pas convaincu. Les résultats positifs concordants obtenus par une immunothérapie de transfert de cellules effectrices spécifiques du système immunitaire au patient ont fait que la communauté des médecins et immunologistes s’est convertie à l’importance du rôle antitumoral du système immunitaire.