Evolution virale et menace pandémique
Un individu qui a été infecté développe une mémoire immunitaire, cette mémoire lui permet (pendant quelques années ou une vie entière), de combattre efficacement le virus s'il l'infecte à nouveau. Mais cela n'est valable que si le virus (ou tout autre agent infectieux) reste identique. S'il "évolue" la mémoire immunitaire ne le reconnait plus et les défenses immunitaires deviennent moins efficaces. Dans ce cas c'est toute une population qui n'est plus protégée. C'est d'ailleurs pour cette raison qu'il faut renouveler chaque année la composition du vaccin contre la grippe, il faut adapter le nouveau vaccin au nouveau virus grippal circulant.
Dans le cas du virus H5N1, les déterminants antigéniques sont les protéines de surface H5 et N1, ces protéines peuvent évoluer de façon infime ou radicale. Les modifications potentielles de ces antigènes résultent de modifications ou mutations des gènes qui codent ces deux protéines. Ainsi l'apparition d'un virus grippal d'un sous-type inconnu de la population humaine comme le H5N1, rend innefficace la mémoire immunitaire de la population générée au cours des épidémies saisonnières dues aux virus grippaux classiques ( H3N2 et H1N1). Ce virus pandémique capable d'infecter les cellules humaines et de se transmettre d'homme à homme n'existe pas encore. Les spécialistes ne sont pas en mesure de prédire sa virulence c'est à dire si cette virulence sera identique à celle de la grippe espagnole de 1918 ou identique à celle d'une grippe hivernale classique.
Quels sont les mécanismes à l'origine de l'évolution des virus grippaux et donc du virus de la grippe aviaire H5N1?
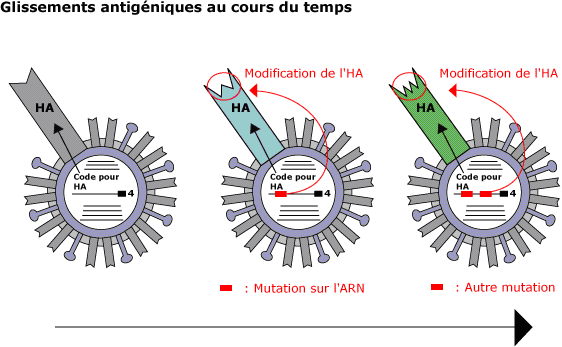
- Les glissements antigéniques
On parle aussi de dérive génétique. Il s'agit de mutations ponctuelles réalisées par l'ARN polymérase, enzyme qui recopie les segments d'ARN avec, souvent, des erreurs qui ne sont pas corrigées. Toutes les erreurs commises demeurent (l'ARN est ensuite copié en ADN). Les mutations peuvent être silencieuses c'est à dire qu'elles n'entraînent aucune modification des acides aminés codés. Parfois au contraire elles engendrent des changements dans la séquence des acides aminés constituant les protéines. Celles-ci sont parfois délétères pour le virus, ou parfois elles sont bénéfiques, c'est ce qui se passe quand une mutation affecte une protéine antigénique portée par le virus. Le système immunitaire de l'hôte qui le porte, ne le reconnait désormais plus.
Le taux de mutation du gène codant l'hémagglutinine est 1000 fois supérieur au taux de mutation observé lors de la synthèse des protéines dans les cellules chez les mammifères. Ce mécanisme explique que d'une année sur l'autre la séquence des gènes de l'hémagglutinine des virus de la grippe A humaine varie d'environ un pour cent.
Ce mécanisme qualifié de "glissements antigéniques" ne conduit qu'à des modifications mineures du génome viral. Par glissement, apparaissent ainsi au sein des virus Inflenza de type A de nombreux variants, c'est le cas par exemple de la souche grippale H3N2 apparue au cours de l'hiver 2003-2004 et dérivant d'une souche H3N2 de 1968. Tous les ans, des épidémies de grippe touchent ainsi une fraction de la population ne présentant aucun système immunitaire adapté.
 |
| D'après www.science.gouv.fr |
- Les cassures antigéniques
La cassure antigénique ou réassortiment génétique peut conduire à un changement total des protéines de surface du virus. On parle alors de virus hybride, il serait :
- humain à l'intérieur c'est à dire que toutes les protéines internes, nécessaires au cycle cellulaire sont celles de virus grippaux humains
- non humain à l'extérieur, c'est à dire qu'au moins une des protéines de surface, par exemple l'hémaglutinine, sera complètement inconnue de l'homme: le virus présentera en surface une hémagglutinine d'oiseau n'ayant encore jamais circulé chez l'homme.
Ce virus hybride serait le résultat d'échanges entre les segments d'ARN de deux virus différents l'un aviaire et l'autre humain ayant co-infecté une même cellule. Ce virus réassortant est "humain" dedans et "oiseaux" dehors, il conserve sa capacité de multiplication chez l'homme mais n'est pas détecté par le système immunitaire humain.
Le porc "hôte intermédiaire" |
Le réassortiment permet de produire des variations génétiques importantes. Le virus de la grippe contient 8 segments d'ARN dont l'un ou plusieurs peuvent provenir d'un autre virus. Lors d'une co-infection d'une cellule porcine par exemple avec un virus avaire et un virus humain il peut y avoir des mélanges de segments d'ARN entre les deux virus. Ces modifications radicales appelées aussi "saut antigénique"ne concernent que les virus de type A, ces échanges portant sur les gènes de l'hémagglutinine et/ou de la neuraminidase se font avec des virus influenza A animaux des porcs, des chevaux, ou des oiseaux aquatiques. Ce mécanisme a fait apparaître autant de sous-types différents capables de générer une pandémie.
C'est le cas observé pour l'hémagglutinine du virus de 1918 qui dérive à la fois du virus de la grippe porcine et du virus de la grippe humaine. Ce nouveau virus a ainsi échappé à la reconnaisssance du système immunitaire humain et créé les dégâts que l'on connaît.
Les pandémies de grippe de 1957 et de 1968 résultent de l'émergence d'un virus résultant d'un réassortiment entre virus aviaire et humain: par exemple en 1957, le virus A/H2N2 adapté à l'homme résulte de l'assemblage des segments de gènes PA, PB2, NP, M et NS provenant d'un virus humain A/H1N1 avec les segments des gènes PB1, Ha, Na provenant d'un virus aviaire A/H2N2. Ce réassortiment s'est opéré chez le porc.
- Perte de la mémoire immunitaire
Une autre possibilité est que la circulation d'un virus dans la population humaine s'arrête pendant plusieurs années. La réponse immunitaire s'amenuiserait alors progressivement. Si cette souche virale perdure dans une population animale et qu'un contact ultérieur avec l'homme ait lieu, alors l'animal pourra transmettre le virus. C'est le cas enregistré avec le virus de la grippe espagnole H1N1, il a disparu de la population humaine vers 1957, il est pourtant resté chez le porc ce qui lui a permis de réapparaître 20 ans plus tard en 1977.
