B- Généralités sur l'IRM
Télécharger le document en version .doc
La neuro imagerie : des images comme modèle
L’ambition des neurosciences cognitives est de faire correspondre à des activités complexes (souvent définies par l’approche psychologique en terme de résolution de problème : compréhension et production du langage, reconnaissance de formes, de visages, identification du sens d’un objet, formulation d’une intention…) des corrélats d’activité physiologique. Une fonction cognitive peut être définie comme une séquence temporelle d'activités neuronales, électriques et neurochimiques, distribuées en réseau, et engendrant des variations locales à la fois du champ électro-magnétique, du métabolisme énergétique, et du débit sanguin cérébral (DSC).
L’imagerie par résonance magnétique (IRM), généralités
L'IRM permet d'obtenir des images numériques en trois dimensions d'une précision inférieure au millimètre, du cortex, de la substance blanche, du liquide céphalo-rachidien et des noyaux gris centraux.
Le sigle IRM regroupe en fait un ensemble de techniques d'imagerie : outre des images anatomiques et fonctionnelles, l'IRM permet d'obtenir des images de l'organisation spatiale des vaisseaux cérébraux (angiographie IRM), de l'orientation des principaux faisceaux de fibres blanches ( IRM de diffusion) , de la distribution de sang ( IRM de perfusion) ainsi que de la concentration locale de certains métabolites énergétiques et peut-être, bientôt, de certains neurotransmetteurs ( spectroscopie IRM). C’est au début des années 70, grâce aux travaux du chimiste américain Paul Lauterbur et du physicien britannique Peter Mansfield – lauréats du Prix Nobel de médecine 2003 – ainsi que Raymond Damadian, que l’imagerie par résonance magnétique trouve un débouché médical.
Principe de l'IRM
L'IRM consiste à observer les tissus biologiques à travers les propriétés magnétiques de l'un de leurs constituants majoritaires, le noyau d'hydrogène. En effet, le proton qui constitue le noyau de l'atome d'hydrogène possède, du fait de sa charge et de son mouvement de rotation sur lui même, un moment magnétique dit de spin, c’est à dire qu’il se comporte comme une sorte de petit aimant. Lorsque l'on place un sujet dans un champ magnétique intense noté "vecteur Bo", les spins des noyaux d'hydrogène s'orientent dans la direction de ce champ. Tout se passe comme si on "aimantait" le sujet.
|
Imageur BRUKER MEDSPEC 30/80 AVANCE - Aimant à haut champ : 3 Tesla (Sensibilité à l’activité cérébrale) Système de gradients très puissant (45mT/m) (Résolutions spatiale et temporelle) D’après J.L. Anton, IRMf MarseilleJournée IRM fonctionnelle - Marseille - 3 octobre 2002 |
En fait, en IRM, on mesure avant tout la relaxation de cette aimantation, après le phénomène de résonance magnétique. La résonance magnétique est obtenue en appliquant une radiofréquence (champ électromagnétique en rotation ->B1) dont la fréquence de précession (ou rotation) f0 est caractéristique d’un atome donné dans un environnement moléculaire donné selon l’équation fondamentale de la résonance magnétique : f0=ω0/2π=γ.B0/2π
où ω0 est la fréquence angulaire de précession du champs de radiofréquence autour de l’axe longitudinal défini par le vecteur Bo, et γ est le rapport gyromagnétique du noyau considéré. Ce rapport γ étant spécifique pour une espèce nucléaire donné, il constitue une forme de signature atomique. L’application d’une radiofréquence confère donc à chaque proton une aimantation M ayant une composante longitudinale (Mz, selon l’axe du champ principal vecteur Bo) et une composante transversale (Mxy) qui lui est perpendiculaire. Lorsque l’application de la radiofréquence est interrompue, cette aimantation va disparaître c’est à dire que les protons recouvrent leurs spins initiaux. Ce phénomène est appelé relaxation. L’onde radiofréquence est appliquée grâce à une antenne située à l’intérieur de l’aimant principal et qui sert également d’antenne réceptrice.
| Lorsqu’un proton est placé dans un champ magnétique intense Bo, il acquiert une aimantation M (dite longitudinale, ici selon l’axe z). Si on applique également une onde radiofréquence, c’est à dire un champ magnétique tournant B1 autour de l’axe z avec une vitesse angulaire ω0 telle que ω0=γ.B0 (condition de résonance), alors l’aimantation du proton acquiert une composante transversale (Mxy) |
Un des avantages de l'IRM réside donc dans le fait que selon les réglages de la même machine, et particulièrement de la séquence d’acquisition (décourt temporel de l’application des radiofréquences), on peut isoler un facteur participant au contraste de l’image. On peut acquérir différents types d'images correspondant à différents types de signal local. Ainsi les images dites « pondérées en T1 » sont souvent utilisées pour l'anatomie, dans la mesure où la séquence d’acquisition favorise la détection de l’eau peu mobile c’est à dire intracellulaire (signal élevé pour la substance grise et faible pour les os par exemple).
De la même manière les images dites « pondérées en T2 ouT2* » sont utilisées commes images fonctionnelles dans la mesure où la séquence d’acquisition favorise la détection de l’eau mobile c’est à dire extracellulaire ou intravasculaire, ce qui constitue une approche du débit sanguin cérébral local.
|
Les courbes représentent l’évolution de l’aimantation à de l’application de la radiofréquence et après son arrêt.Cette évolution est différente selon les tissus (Fat : graisse, WM : substance blanche, GM : substance grise, CSF : compartiment intravasculaire). La pondération en T1 (pointillé rouge) permet de visualiser surtout les compartiments dont la variation d’aimantation est rapide (Fat, WM, GM), c’est à dire les structures anatomiques.La pondération en T2 (pointillé blanc) permet de visualiser surtout les compartiments dont la variation d’aimantation est lente. (compartiment intravasculaire), comme le CSF. D’après Dojat, 2003 |
- T1, T2, T2* sont les paramètres de relaxation
- dans la pratiques des agents de contraste ayant des propriétés paramagnétiques (tels que le Gadolinium) sont utilisé pour augmenter le contraste du signal IRM.
- le codage spatiale des images IRM est réalisé en appliquant un gradient de champ magnétique sur la préparation.
L'IRM fonctionnelle
L'IRM fonctionnelle est fondée sur l'observation en temps réel des variations de l'oxygénation du sang et des débits sanguins cérébraux locaux, sans injection de traceur radioactif, puisque le traceur est endogène. Des examens répétés peuvent, de ce fait, être réalisés sans aucun inconvénient c’est à dire de manière non invasive. L'oxygène, libéré au niveau des capillaires cérébraux, entraîne la réduction du fer qui se retrouve à l'état d'ion ferreux ( Fe2+), laissant deux électrons non appariés au sein de la molécule de déoxy-hémoglobine (dHb). Ces électrons sont à l'origine du paramagnétisme de cette molécule et génèrent une modification du champ magnétique local. La désoxyhémoglobine se comporte comme une hétérogénéité magnétique. L’augmentation de la concentration locale en dHb entraîne ainsi une atténuation du signal IRM dans les zones (voxels) contenant du sang desoxygéné. Alors que l'oxy-hémoglobine n'a aucune influence sur le champ magnétique local.
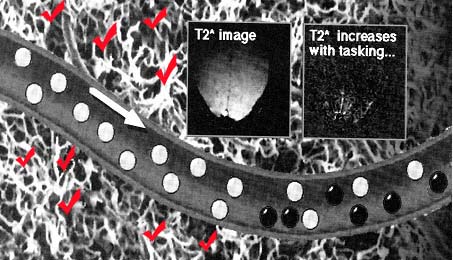 |
|
| Faible activité neuronale, Débit sanguin cérébral normal, signal IRM faible du fait de la présence de dHb. |
Forte activité neuronale, Débit sanguin cérébral élevé, Réduction du taux de dHb Augmentation du signal BOLD |
Principe de construction des images cérébrales
L'IRMf permet ainsi de localiser dans un cerveau les zones mises en jeu (activées) par la réalisation d’une tache simple.
|
1ère étape : Obtention d’une image anatomique de bonne résolution avec pondération en T1. (Brett & al., 2002) |
|
2eme étape : Obtention d’images fonctionnelles avec pondération en T2*Traitement d'une série d'image pour extraire le signal du bruit. Image de soustraction des images obtenues selon les modalités on/off ou on/aléatoire des paradigmes expérimentaux.Traitement statistique pour éliminer les faux positifs et faux négatifs. (Brett & al., 2002) |
| D’après Brett & al., 2002 |
La production d’images cérébrales est donc une construction complexe issue d’une analyse statistique importante et qui a bénéficié du développement des capteurs et des techniques d’acquisition et de traitement informatique du signal et de l’image.
Au delà des difficultés relatives à l’acquisition et au traitement du signal, la construction même des images cérébrales est étroitement dépendante du paradigme utilisé pour activer le cerveau. L’une des principales difficultés consiste à isoler l’opération cognitive que l’on veut étudier du reste de l’activité cérébrale. Idéalement, il s’agit donc d’éliminer toutes les activités cérébrales non spécifiques à l’opération étudiée. Les techniques d’imagerie cérébrale fonctionnelle permettent alors d’identifier les régions du cerveau dont le débit sanguin cérébral a été modifié de façon significative au cours de l’exécution de la tâche.
Plusieurs protocoles ou paradigmes de construction d’images cérébrales sont utilisés. Le plus simple est sans doute le paradigme en bloc dit de soustraction ou de différence. Elle n’est utilisée que dans des protocoles expérimentaux simples (identification des aires sensorielles et motrices primaires par exemple).
L’activité cérébrale est enregistrée au cours d’une condition neutre (ou de référence R) où le stimulus est présenté sans instruction particulière. Un deuxième enregistrement est effectué mais dans la condition dite cible. L’activité résultant de l’opération étudiée correspond à la « soustraction » de la mesure en condition cible par la mesure en condition neutre. Cette soustraction correspond à un test de différence statistique significative (test T par exemple) appliqué voxel à voxel et dont on peut faire varier le seuil.
|
Mesure de la variation du signal RMN au cours du temps au niveau du cortex visuel dans une situation de stimulation lumineuse intermitente (Off : obscurité, condition de référence ; On :stimulus visuel, situation cible) D’après Kwong & al. 1994
|
Les contraintes expérimentales
La mise en oeuvre d'un protocole expérimental en IRM pose un certain nombre de problèmes liés:
- à la nécessité de travailler en présence d'un fort champ magnétique ( d'où des règles de sécurité très strictes )
- au confinement du sujet dans l'imageur IRM ( intervention de l'état psychique des patients)
- au bruit important généré par les bobines de gradients pendant l'acquisition des images ( ce bruit d'origine mécanique constitue une interférence relativement importante dans le protocole expérimental, que les systèmes de casques ou de bouchons auditifs ne viennent qu'imparfaitement atténuer, et dont il faut tenir compte lors de l'interprétation de certaines données ).
Lire et interpréter une image cérébrale
Dans le cadre de l’IRM, une image peut être définie comme « un ensemble de points ou d’éléments (pixels pour une image 2D, voxels pour une image 3D) représentatifs de l’apparence d’un objet formé à partir du rayonnement émis, réfléchi, diffusé ou transmis par cet objet ». Dans le cas de l’IRM, la discrétisation du signal par un convertisseur analogique-digital permet d’obtenir une image de type numérique, c’est à dire le codage informatique d’un signal physique. L’image est donc décomposée en un ensemble de points auxquels son associées des intensités de signal, en général codées grâce à une échelle de couleur. Les caractéristiques de l’image sont :
- sa taille (« field of view » ou FOV en anglais)
- sa résolution (nombre de points ou pixels décrivant l’objet
- le contraste, c’est à dire la différence de signal détectable entre deux points
Les images cérébrales correspondent à des construction de coupe transversale, sagittale (longitudinale), coronale de l’encéphale ou d’un seul hémisphère, elles peuvent également représenter le cerveau dans sa totalité. La première étape de la lecture de l’image consiste donc à repérer le type de construction auquel on a à faire de manière à orienter celle ci (partie postérieure / antérieure, gauche / droite). Certaines structures facilement repérables (cervelet, scissure de Sylvius, corps calleux…) permettent, avec un peu d’habitude, de réaliser ce repérage.
Il est ensuite nécessaire d’identifier :
- s’il s’agit d’une image individuelle ou d’un moyennage d’images interindividuelles
- s’il s’agit d’images composées directes ou d’images de différences ou de corrélation ou d’interaction, c’est à dire de savoir à quel paradigme expérimental correspond l’image proposée.
Dans le cas d’une image de différence (cas le plus fréquent), il est nécessaire d’identifier l’opération cognitive qui a été isolée au cours du protocole de manière à pouvoir exploiter la signification fonctionnelle de l’image.
Enfin les images cérébrales sont traitées à l’aide d’un code de couleur. L’échelle d’activité correspondant à ce code n’est pas toujours présente. En général les couleurs les plus chaudes (jaune, rouge) correspondent à des activités importantes et les couleurs froides (bleu) à des activités faibles.
Bibliographie générale :
Jeannerod Marc, 2002, « Le cerveau intime », Paris, CSI, Ed. Odile Jacob.
Mazoyer B., Belliveau J.W., 1996, « Les nouveaux progrès de l’imagerie » in La Recherche n° spécial 289, Juillet-Aout 1996, pp26-33.
Vion-Dury J., 2002, « Cours de résonance magnétique, spectroscopie et imagerie », Ellipses.
Rosenzweig M.R., Leiman A.L., Breedlove S.M., 1998, Psychobiologie, De Boeck Université
Segebarth C., Ziegler A., (unité mixte UJF - Inserm U594 / IFR1), Journées de formation « Introduction à la neuroimagerie fonctionnelle et métabolique par RMN », Grenoble, 21-26 Novembre 2003.
+ neurosciences cognitives
Référents scientifiques :
Jean Luc Anton, Ingénieur de recherche, Centre IRMf, CHU Timone, MARSEILLE
Segebarth Christoph, Directeur de Recherche, INSERM U 594- Université Joseph Fourier (UJF),
Neuroimagerie Fonctionnelle et Métabolique, GRENOBLE
Michel Dojat, Ingénieur de recherche, INSERM U 594- Université Joseph Fourier (UJF),
Neuroimagerie Fonctionnelle et Métabolique, GRENOBLE
