Commentaire 6. Bilan sur le mécanisme d’action des récepteurs CAR des cellules CAR-T
II - Une immunothérapie récente : Les cellules CAR-T
La liaison entre le scFv d’un récepteur CAR d’une cellule CAR-T anti-CD19 et l’antigène CD 19 d’une cellule tumorale d’une LAL est visualisée par la figure du document 14a. Cette liaison qui traduit la reconnaissance de la cellule tumorale par la cellule CAR-T est le premier mécanisme en jeu.
Le document 14a montre aussi la partie intracellulaire du récepteur CAR.
Le fichier de séquences fournit les séquences du la protéine CD3 zeta et de la protéine co-stimulatrice CD28 d’un lymphocyte CD8 cytotoxique. Ces deux molécules sont impliquées dans l’activation du lymphocyte suite à la reconnaissance spécifique de l’antigène par le récepteur TCR.
La comparaison de la séquence du CAR anti-CD19 avec les séquences CD3 zeta et CD28 du lymphocyte T cytotoxique est illustrée par le document 14b. Elle traduit la présence dans la partie intracellulaire du CAR de ces séquences activatrices. Ce mécanisme (complexe) est le deuxième processus intervenant dans l’action de la cellule CAR-T.
La figure ci-dessous traduit la modalité effectrice de la cellule CAR-T sur la cellule tumorale engendrée par son activation (perforine, granzymes, cytokines pro inflammatoires, IL2, interféron gamma, TNF alpha). Cette figure donne aussi une vue d’ensemble des mécanismes de la cellule CAR-T contre la cellule tumorale.
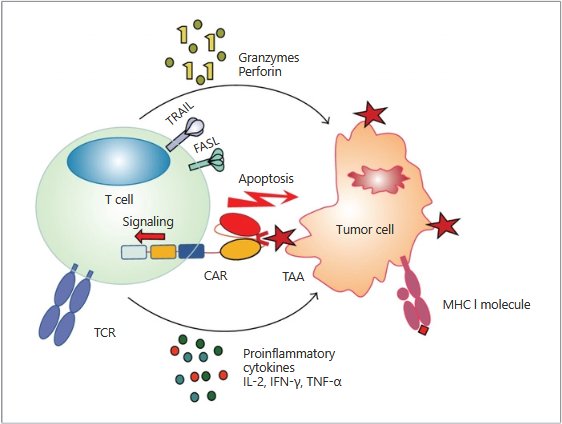
Source : M.N. Metzinger et al. Chimeric antigen receptor T celltherapy : Reach to solid tumor experience. Oncology 2019.
La figure du document 15 fait la synthèse des informations extraites des documents précédents en mettant en évidence les caractéristiques essentielles de la constitution d’un récepteur CAR. Elle indique que le CAR a deux origines : celle d’un anticorps spécifique d’un antigène tumoral pour sa partie extracellulaire, celle d’un lymphocyte T pour sa partie intracellulaire. Cela justifie le qualificatif de « chimérique ».
Le domaine scFv extracellulaire du CAR comprend les fragments variables d’une chaîne légère et d’une chaîne lourde de l’anticorps membranaire dont il dérive. Par ce scFv, le CAR reconnaît et se lie à l’antigène tumoral comme le fait l’anticorps sans présentation par les molécules du CMH. C’est une différence fondamentale avec le TCR d’un lymphocyte T Cytotoxique qui fait que la cellule CAR-T peut agir sur la cellule tumorale qui échappe à l’action effectrice des lymphocytes T CD8.
La partie intracellulaire du CAR comprend des protéines qui interviennent dans l’activation du lymphocyte TCD8 cytotoxique suite à la reconnaissance de l’antigène. Celle de la cellule CAR-T est semblable et se traduit par la formation d’une synapse immunologique qui induit la destruction de la cellule tumorale.
L’image du document 16 montre que l’évolution de la structure des récepteurs synthétiques CAR conçue par les généticiens immunologistes et les cliniciens n’a pas porté sur le domaine de reconnaissance de l’antigène tumoral mais sur le domaine intracellulaire du récepteur. Toutefois, si la structure du scFv est restée la même, il y a eu production de différents types de cellules CAR-T en fonction de la nature de l’antigène tumoral. Une des difficultés réside d’ailleurs dans l’identification d’un antigène spécifique des cellules d’une tumeur.
Les CAR dits de première génération des CAR-T avaient un domaine intracellulaire constitué uniquement par la chaîne activatrice CD3 zeta. L’absence de facteurs de costimulation (comme CD28) avait pour conséquence une faible réponse antitumorale, une prolifération réduite in vivo et une durée de vie assez courte des CAR-T au sein de l’organisme des patients. L’évolution des récepteurs CAR a consisté en l’insertion de facteurs de costimulation, d’abord un seul (CD28 ou 4-1BB), puis deux ou plusieurs. Des évolutions sont encore en cours et certaines au stade d’essais précliniques.
La majorité des essais cliniques qui sont rapportés et dont les résultats sont positifs ont été réalisés avec des CAR de deuxième génération (comme par exemple l’essai clinique rapporté sur la leucémie aigüe lymphoblastique (LAL)). Les CARs de troisième génération s’avèrent plus efficaces et diminuent les effets secondaires nocifs de ce type de thérapie.
