Résultats d’un essai clinique
II - Une immunothérapie récente : Les cellules CAR-T
3 - Résultats d’un essai clinique
Dans un article de 2018 paru dans le « New England Journal of Medicine » une équipe de médecins rapporte les résultats d’un essai clinique d’immunothérapie réalisé en utilisant des cellules CAR-T. Ce sont les résultats de cet essai qui ont conduit la « Food and Drug Administration » des USA à autoriser ce traitement qualifié de « médicament vivant » contre certains cancers, notamment la leucémie aigüe lymphoblastique (LAL) et les lymphomes.
Cet essai clinique a porté sur 75 patients (enfants et jeunes adultes) atteints d’une LAL réfractaire à tous les protocoles de chimiothérapies. La LALB de ces patients est due à une multiplication incontrôlée des lymphoblastes de la moelle osseuse, précurseurs immatures des lymphocytes B.
Le document 11 est celui d’un frottis de moelle osseuse d’un patient LAL où les cellules ont été colorées par la méthode de May-Grunwald-Giemsa. Dans un frottis normal, le pourcentage des lymphoblastes est compris entre 1 et 5%. En cas de LAL, il peut atteindre 80%. Ces lymphoblastes peuvent passer dans le sang et être détectés sur un frottis sanguin. La conséquence de cette prolifération des lymphoblastes est une diminution des autres cellules sanguines : hématies, polynucléaires, plaquettes, à l’origine des signes pathologiques de la LAL.
Document 11 : Frottis de moelle osseuse en cas de LAL
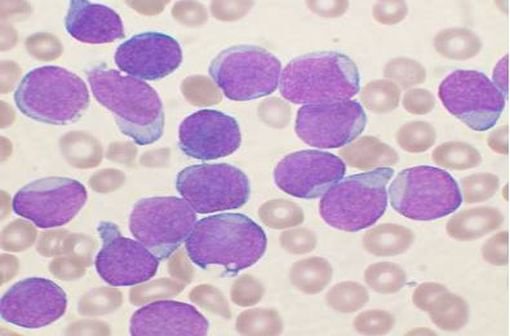
Source : VIDAL. Frottis de moelle osseuse d'un patient atteint d'une leucémie lymphoblastique aiguë à cellules B (illustration @VashiDonsk sur Wikipédia anglais).
81% de ces 75 patients (61 sur 75) sont entrés en rémission, c’est-à-dire avec une moelle osseuse ayant retrouvé une structure normale. 58 de ces 61 étaient déjà en rémission le 28ème jour après l’infusion des cellules CAR-T. Trois mois après le début du traitement, 45 des 61 en rémission complète avaient une formule sanguine normale tandis que celle de 16 d’entre eux présentait des anomalies résiduelles.
La rémission a été durable pendant les deux ans de l’étude. Elle a été associée avec la persistance de cellules CAR-T. Le nombre de cellules CAR-T a été maximum une dizaine de jours après l’infusion des CAR-T.
Pistes de questionnement :
- Expliquer en quoi ces données montrent que les cellules CAR-T ont une action antitumorale plus efficace que les lymphocytes T CD8 cytotoxiques.
- Expliquer comment la rémission s’accompagne de la disparition de signes cliniques de la maladie : fatigue, sensibilité aux infections, hémorragies diverses, se traduisant par l’apparition de « bleus ».
 |
