Les traitements antiviraux et les vaccins
Les traitements antiviraux
Les médicaments antiviraux visent à perturber une étape du cycle de réplication des virus en général. Dans le cas des virus grippaux et en particulier celui du H5N1, les cibles les plus interessantes sont celles situées en surface du virus c'est à dire la neuraminidase et la protéine M2.
- Les inhibiteurs de la neuraminidase (Na)
Il s'agit de médicaments qui agissent sur la neuraminidase des virus grippaux. Ils bloquent spécifiquement l'action enzymatique de la neuraminidase virale et protègent ainsi les membranes des cellules des muqueuses supérieures animales et humaines de l'attaque de nouveaux virus.
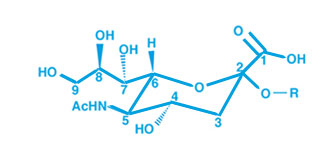
Les médicaments antiviraux INa (Inhibiteur de la Na) sont des molécules dont la conformation spatiale mime celle de l'acide sialique des cellules des voies respiratoires, substrat de la neuraminidase.
L'inhibiteur vient se fixer sur le site actif de la neuraminidase bloquant ainsi sa liaison à l'acide sialique de la cellule cible et donc son activité. En effet, sans l'action de la neuraminidase les virions ne sont pas détachés de la cellule hôte dont ils sont issus et sont incapables d'infecter d'autres cellules. Les virus ainsi neutralisés sont exposés aux anticorps qui vont les éliminer.
VIDEO: action d'un INa comme l'oseltamivir (La grippe en face, Yves Buisson, Elisabeth Nicand et Pierre Saliou, Edition Xavier Montauban, avec aimable autorisation de l'éditeur)
La neuraminidase est une cible privilégiée par les laboratoires pharmaceutiques car la structure de son site actif est toujours bien conservée au fil des générations virales successives.
L'une de ces molécules inhibitrice Ina est l'oseltamivir contenue dans le médicament "Tamiflu" dont l'autorisation de mise sur le marché (AMM) a été accordée en 2001. Cet antiviral est actif sur tous les sous types de la neuraminidase du fait de la grande stabilité de ce site actif. Le facteur déterminant de l'efficacité du traitement est le délai du début du traitement par rapport à la date de l'infection. Il devrait être instauré dans les douze premières heures suivant l'apparition de la fièvres. Au delà il ne ferait que ralentir la progression du virus dans l'organisme mais ne guérirait pas. En effet ces médicaments n'ont aucun effet au sein des cellules déjà infectées, il faut attendre la mort de la cellule infectée pour que les virus multipliés en grand nombre puissent alors être neutralisés.
 |
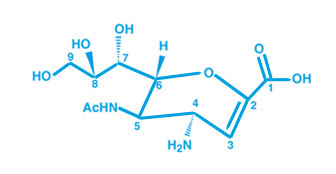 |
| Acide sialique | Oseltamivir |
|
D'après La grippe en face, Yves Buisson, Elisabeth Nicand et Pierre Saliou, Edition Xavier Montauban, avec aimable autorisation de l'éditeur) |
|
Le Tamiflu est devenu le médicament de choix pour les gouvernements et l'OMS dans leur préparation à une possible pandémie de grippe aviaire (après recombinaison du H5N1 avec un autre virus grippal affectant l'Homme)
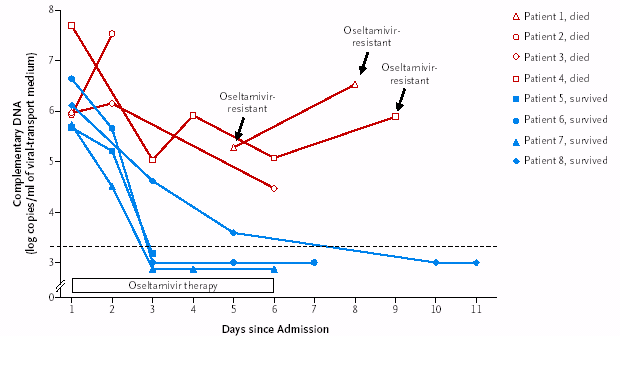
Cependant, des données cliniques récentes relevées chez plusieurs malades atteints du A/H5N1 de clade 1 en 2005 au Vietnam et traités au Tamiflu révèlent (voir les graphes ci-dessous) une résistance à l'Oseltamivir. La dose administrée avait été insuffisante favorisant ainsi l'émergence de virus mutants résistants.
| Sensibilité de H5N1 à l'Oseltamivir, d'après N Eng J Med 2005;353:2333-6 |
 |
|
Tous les individus reçoivent de l'Oseltamivir pendant 6 jours. On note le nombre de copies ARN du virus H5N1 chez ces individus au cours des jours de traitement et des 5 jours qui suivent. |
Les souches isolées chez les patients traités sont rares et présentent des mutations variées mais uniquement situées au niveau du site actif de la neuraminidase. Les INa ne devraient être utilisés que lorsque les symptômes sont apparus depuis moins de 48 heures et de préférence depuis moins de 12 heures. La durée de traitement doit être au moins de cinq jours voire plus pour les personnes à risque. Le détail de la prescription du Tamiflu est référencée dans le Vidal (http://www.vidal.fr).
- Les inhibiteurs de la protéine virale M2
La protéine M2 agit comme une pompe à protons qui régule le pH interne du virus. Un pH bas est nécessaire pour son encodage. Le blocage de la protéine M2 entraine l'arrêt de la réplication virale au stade précoce de l'infection.
Deux médicaments contiennent des molécules bloquant la M2, l'Amantadine (Mantadix) et la Rimantadine (Roflual), ils sont peu onéreux, contrairement au Tamiflu.
Les inhibiteurs de la M2 sont des molécules à 10 atomes de carbone, en forme de cage et portant un groupement aminé, propriété indispensable à leur activité antivirale. Ils se fixent sur la région du pore ménagé par la canal empêchant ainsi le transfert d'ions à travers la membrane virale ou de l'endosome. La phase de décapsidation et donc de sortie du génome viral est empêchée.
Ces inibiteurs de la M2 sont actifs sur les virus de type A H3N2, H1N1 et H2N2. Leurs effets sur les souches virales de A/H5N1 de clade 1 et celles de clade 2.1 circulant actuellement dans le sud-est asiatique sont peu concluants en effet une mutation observée sur l'acide aminé en position 31 de cette souche, où une sérine est remplacée par l'asparagine, confère toujours une résistance à l'amantadine. Le détail de la prescription du Mantadix contenant l'amantadine est détaillée dans le Vidal (http://www.vidal.fr).
Les vaccins
La vaccination des oiseaux apparait comme la mesure indispensable pour contrôler l'extension d'une épidémie surtout dans des pays où l'application stricte des mesures d'hygiène et de sécurité agricoles restent aléatoires. On dispose actuellement pour les oiseaux de différents vaccins. Un vaccin inactivé dirigé contre le virus asiatique A/H5N1 élaboré en 2005 confère une protection de 100%.
La perspective d'une vaccination humaine est encore de l'ordre de la recherche. Un certain nombre d'essais cliniques à partir de souches virales H5N1 circulant dans le sud est asiatique sont en cours:
|
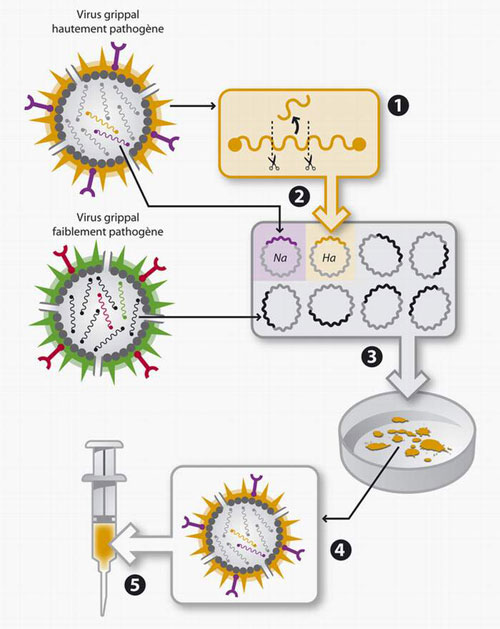
Principe de la génétique inverse |
||||||||||
|
- en décembre 2005 Sanofi pasteur a débuté des essais sur un vaccin contre le H5N1 et aujourd'hui participe à la production d'un vaccin contre la souche H7N1 à fort potentiel pandémique
- actuellement le Japon teste un vaccin chez l'homme
- en mai 2006 l'OMS annonce que de nouvelles formes du virus ont émergé en Asie, elles sont distinctes des deux souches vacciniques développées par l'OMS en 2003 2004 à parir des virus H5N1
- en aout 2006 l'OMS a recommandé un choix de virus candidats pour un vaccin pré-pandémique.
- différents pays travaillent actuellement sur des projets de vaccins, les vaccins candidats contre les souches H7 et H9 sont testés chez l'homme, à noter les travaux du loboratoire Chiron. Des essais cliniques sont actuellement en cours.
Recherche sur un vaccin antigrippal universel: une équipe belge annonce avoir expérimenté avec succès un prototype de vaccin universel contre toutes les formes de grippes y compris le H5N1 et la grippe saisonnière. Ce vaccin vise l'antigène M2 présent sur toutes les formes de virus grippaux, cette protéine reste stable chez les différents variants de la grippe. Ce vaccin assurerait une immunité durant 10 ans. Les chercheurs belges attendent un soutien dans leurs recherches par les fonds publics européens et par l'OMS. Un tel vaccin constituerait une avancée majeure en terme de santé publique humaine et vétérinaire à l'échelle mondiale.
Les vaccins contre un potentiel candidat H?N? ne sont qu'à un stade précoce de développement.
Le virus aviaire A/H5N1 est actuellement le candidat le plus redouté pour déclencher la prochaine pandémie. La France a réservé 40 millions de traitements vaccinaux mais ce vaccin pandémique ne sera disponible qu'après trois ou six mois c'est à dire très probablement après la première vague de la pandémie. Etant donné la faible disponibilité du vaccin, les personnels de santé naturellement en première ligne, les enfants et les personnes particulièrement vulnérables seront prioritaires. L'expérience des situations passées indique que la vaccination des personnes les plus susceptibles d'infecter les autres semble être le moyen le plus efficace pour développer une immunité collective et casser la dynamique de l'épidémie.
Combinaison de différents moyens de lutte
Face à une pandémie, les modèles mathématiques développés indiquent qu'il est nécessaire de conjuguer différents moyens pour réduire les conséquences.
- emploi d'antiviraux en diminuant l'infectiosité des malades et en protégeant les personnes en contact
- le port du masque et l'ensemble des mesure barrières
- la vaccination (prépandémique puis pandémique) en développant rapidement une immunité collective