activité 8
Du cycle court au cycle long
Activité 8a : Les phénomènes géologiques qui régissent le cycle du carbone à long terme.
 |
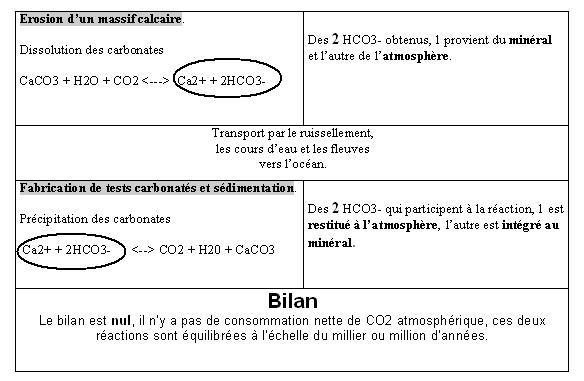 |
Activité 8b : Comment mettre les élèves en activité sur les différences cycle court / cycle long ?
Dosage des HCO3- dans l'eau d'une rivière.
Voici une expérience facile à réaliser pour déterminer la concentration en ions bicarbonates dans une eau de rivière et par suite la vitesse de consommation de CO2 atmosphérique (flux) par l’altération des roches.
Principe
HCO3-+ H+ = H2CO3
[HCO3-] xVo = VexCa
Ainsi, si on connaît Vo, Ca et Ve, on en déduit la "réserve alcaline" d'une eau (le pouvoir tampon), qui dans la plupart des cas (cas de toutes les eaux de rivières françaises se réduit aux seuls ions HCO3-. On détermine une concentration en mol/l, ou plus classiquement en micromol/l (µmol/l).
NB: il est nécessaire de travailler sur de l'eau filtrée et, bien entendu, d'étalonner le pH mètre auparavant.
Grâce à la concentration et une connaissance même approximative du débit de la rivière (facilement estimable sur le terrain), on évalue la quantité de carbone transitant en un point par unité de temps (un flux).
Flux (mol C/an) = [HCO3-] (mol/l) * Débit (l/an)
Le flux spécifique désigne le flux normalisé à l’échelle du bassin versant et s’exprime en mol C/ Km2/an. Il permet de comparer des rivières de tailles différentes. C’est une vitesse de consommation de CO2 par altération des roches dans le cas d’un bassin versant entièrement silicaté.
Pour obtenir des données sur le cours d’eau choisi. La banque de données Hydro RNDE du ministère de l’aménagement et du territoire s’avère très utile. On y trouve notamment le débit ainsi que la surface du bassin versant.
Expérience témoin
Exemple de la Loire
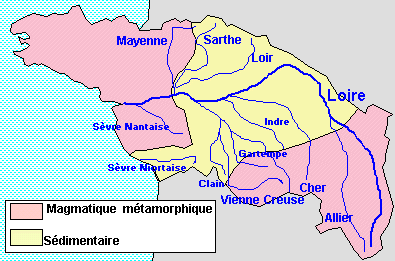 |
|
Géologie du bassin versant de la Loire : 2/3 du bassin est à dominante silicatée, 1/ 3 à dominante calcaire. Surface du bassin à Tours: 42 130 Km2. La moitié du fleuve a évolué sur un substrat silicaté, l’autre moitié sur substrat calcaire. Débit de la Loire : 810 m3/s soit 2.5 * 1010 m 3/an |
|
Matériel nécessaire
|
Mode opératoire
|
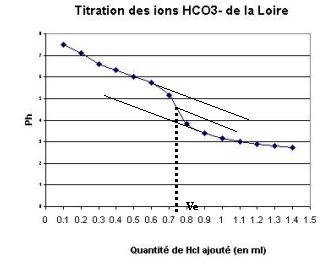 |
La méthode des tangentes permet de déterminer Ve = 0,74ml Ve * [HCl] = Vo * [HCO3-]
[HCO3-] = (0,74*0.1)/40
[HCO3-] = 1,85 * 10-3 moles/L
|
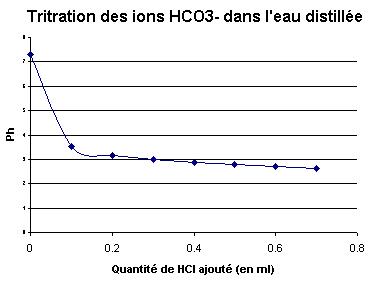 |
Dans le cas de l’eau distillée équilibrée avec l&rsquorsquo;atmosphère, on s’aperçoit qu’il impossible de déterminer le point d’équivalence, le pH de la solution chutant dès le premier ajout d’acide. La quantité de HCO3- est très faible. Il n’est pas possible d’expliquer les concentrations de l’eau de Loire par un simple équilibrage avec le CO2 atmosphérique. Il faut invoquer un mécanisme différent. : l’altération. |
Exercice 1
1.Calculer le flux en moles de CO2/an et le flux spécifique (flux rapporté à la surface du bassin versant) en moles de CO2/km2/an. Exprimer ces deux flux en tonnes de CO2 puis en tonne de C.
Comparaison avec la productivité primaire nette sur le bassin versant
1.Se rendre Sur le SIG en ligne à l’adresse suivante, NDGC.NOAA et déterminer la productivité primaire moyenne nette pour la France, en zoomant sur la zone d’intérêt dans un premier temps, et en utilisant l’outil de sélection par polygone accessible avec l’icône![]()
Délimiter une surface s’apparentant au bassin versant de la Loire et soumettre la requête en utilisant les boutons situés au-dessous de la carte.
2.Comparer avec la consommation de C par l’altération des roches silicatées sur ce même bassin versant. (Il y a 56% de C dans la matière organique produite par photosynthèse)
Activité 8c : Ordre de grandeur de la taille du réservoir carbonaté.
| Équipe INRP de l'académie d'Orléans-Tours. |
